
§ 5. Заполнение энергетических зон электронами
Заполненные уровни создают заполненные зоны, а пустые уровни - пустые зоны. Поскольку энергетические зоны в твердых телах образуются из уровней отдельных атомов, то вполне очевидно, что и заполнение их электронами будет определяться в первую очередь степенью заполненности электронами соответствующих атомных уровней.
Возьмем для примера кристалл лития. В свободном состоянии атомы лития имеют по три электрона. Два из них расположены на 1s-оболочке, полностью заполняя ее. Третий электрон принадлежит 2s-подоболочке, заполняя ее лишь наполовину. Соответственно при образовании кристалла зона 1s оказывается полностью заполненной, а зона 2s - заполненной только наполовину; зоны 2р, 3s, 3р и т. д. в невозбужденном кристалле лития оказываются пустыми, поскольку были пустыми уровни, из которых эти зоны образовались.
Аналогичная картина наблюдается у всех щелочных металлов. Так, при образовании кристалла натрия зоны 1s, 2s и 2р оказываются полностью заполненными, так как в атомах натрия соответствующие уровни полностью укомплектованы электронами (на уровне 1s - два электрона, на уровне 2s - два электрона, а на уровне 2р - шесть электронов). Одиннадцатый электрон в атоме натрия заполняет уровень 3s только наполовину, благодаря этому и зона 3s заполняется электронами наполовину.
При образовании кристаллов из атомов с полностью укомплектованными уровнями создающиеся зоны в общем случае также оказываются целиком заполненными. Так, если бы мы создавали кристалл из атомов неона, то в энергетическом спектре такого кристалла зоны 1s, 2s, 2р были бы целиком заполненными (в каждом атоме неона имеется по 10 электронов, которые и заполняют соответствующие энергетические уровни). Остальные зоны, расположенные выше (зоны 3s, 3р и т. д.), оказались бы пустыми.
Перекрытие энергетических зон в кристалле. В некоторых случаях вопрос о заполнении энергетических зон электронами оказывается более сложным. Это относится к кристаллам щелочноземельных элементов и к кристаллам, имеющим решетку типа алмаза, среди которых наибольший интерес представляют кристаллы типичных полупроводников - кремния и германия.
На первый взгляд кристаллы щелочноземельных элементов должны иметь в энергетическом спектре только заполненные и пустые зоны. В самом деле, атомы, например, бериллия, имеющие по четыре электрона, характеризуются двумя заполненными уровнями 1s и 2s. Атомы магния со своими 12 электронами также имеют заполненные уровни 1s, 2s, 2р и 3s. Однако в кристаллах щелочноземельных элементов верхние энергетические зоны, в создании которых принимают участие заполненные атомные уровни, в действительности оказываются заполненными лишь частично. Объясняется это тем, что в процессе образования кристаллов этих элементов энергетические зоны, соответствующие верхним уровням, размываются настолько сильно, что происходит их перекрытие. В результате такого перекрытия образуются гибридные зоны, в состав которых входят как заполненные, так и пустые уровни. Например, в кристалле бериллия в создании гибридной зоны принимают участие заполненные уровни 2s и пустые уровни 2р (рис. 8), а в кристалле магния - заполненные уровни 3s и пустые уровни 3р. Благодаря эффекту перекрытия верхние энергетические зоны в кристаллах щелочноземельных элементов и оказываются заполненными лишь частично.
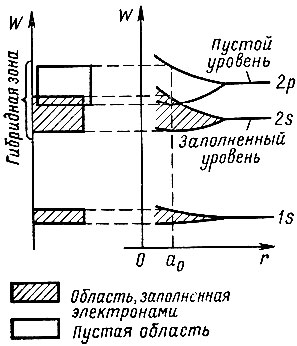
Рис. 8
К совершенно противоположному результату приводит перекрытие зон в кристаллах полупроводников, имеющих решетку типа алмаза. В атомах кремния, например, на уровне 3р (в подоболочке 3р) находятся всего два электрона, в то время как на этом уровне могут расположиться шесть электронов. Вполне естественно ожидать, что при образовании кристалла кремния верхняя энергетическая зона (зона 3р) окажется заполненной лишь частично, в то время как предшествующая ей зона (зона 3s) будет заполнена целиком (она образуется из полностью заполненного уровня 3s). Однако в действительности в процессе образования кристалла кремния эффект перекрытия приводит не только к возникновению гибридной зоны, составленной из подуровней 3s и 3р, но и к дальнейшему расщеплению создавшейся гибридной зоны на две подзоны, разделенные между собой промежутком запрещенных энергий Wg (рис. 9). Всего в гибридной зоне 3s + 3р должно быть по 8 вакантных электронных мест на каждый атом (2 места от подоболочки 3s и 6 мест от подоболочки 3р). При расщеплении же гибридной зоны в каждой из подзон оказывается по 4 места на атом. Стремясь занять нижние энергетические уровни, электроны третьих оболочек атомов кремния (а их всего четыре - два на подоболочке 3s и два на подоболочке 3р) как раз и заполняют нижнюю подзону. Верхняя подзона при этом остается пустой.
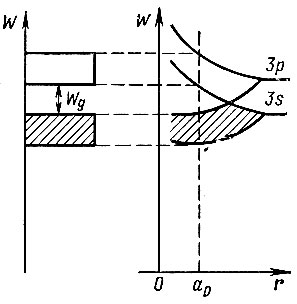
Рис. 9
|
ПОИСК:
|