
ГЛАВА ПЕРВАЯ
На вопрос «Что такое квантовая механика?» ответить осмысленно могут немногие. Все остальные попросту убеждены, что квантовая механика очень трудная наука. Пожалуй, это неправда, но такая уверенность укоренилась не без причин. Логика квантовой механики, по существу, проста, и все же, чтобы привыкнуть к ней, необходимо освоить предварительно несколько понятий, на первый взгляд ничем не связанных между собой. В стройную систему эти понятия складываются не сразу, а лишь при длительном сопоставлении и размышлении.
На это нужны время и силы.
глава первая
Если вы о квантовой механике знаете только то, что она «...разрешила вековую загадку таинственной страны микромира», и еще: «...перевернула все наше мировоззрение», вы знаете о ней примерно столько же, сколько знают туристы о незнакомой стране, путешествующие по ней, не изучив предварительно ее культуру и язык: они видят вокруг людей, которые спешат, смеются, машут руками, но цель их движений туристам неизвестна, а радость — непонятна. В результате же память путешественников сохраняет только яркие пятна реклам на незнакомом языке.
Квантовая механика — обширная страна с богатой и глубокой культурой. Однако, чтобы приобщиться к ней, необходимо изучить ее язык. Язык этот своеобразен, но, в сущности, ничем не отличается от любого иностранного языка. Как и всякий язык, его нельзя усвоить единым усилием воли — необходима система. Для начала нужно просто запомнить несколько ходовых понятий и пытаться строить из них простые фразы, не очень заботясь о строгости грамматических конструкций. Лишь впоследствии придут та легкость и уверенность владения языком, которые приносят с собой ощущение удовлетворения и радости чистого знания.
Вероятно, почти у всех изучение квантовой механики напоминает процесс растворения соли в воде: вначале брошенные в стакан мелкие кристаллы бесследно исчезают, но затем наступает момент, когда достаточно бросить еще один кристаллик, чтобы из раствора на месте этой маленькой затравки стал постепенно расти большой кристалл.
В дальнейшем мы проследим истоки, идеи и находки квантовой механики, объясним систему ее понятий и образов и, наконец, расскажем о приложениях. Но вначале мы должны растворить в своем сознании несколько кристаллов первоначальных понятий, усвоить те несколько необходимых слов, без которых невозможно построить ни одной осмысленной «квантовой фразы». Иногда это бывает утомительно. Но ведь и перед полетом в космос необходимо бегать, приседать и крутиться на центрифуге, а это далеко не самое романтичное занятие. «Для того чтобы мышца развивалась, она должна уставать», — любил повторять знаменитый физиолог Сеченов. Раз навсегда запретив себе утомляться, нельзя понять волнение поисков, радость открытий и тот бескорыстный интерес к важным деталям, который создал, в сущности, не только квантовую механику, но и всю науку.

Интерес
Все это сказано здесь, конечно, не затем, чтобы запугать читателя трудностями в самом начале пути, но посудите сами: ведь не существует таблеток, проглотив которые человек просыпается наутро профессором физики. Для начала мы усвоим три идеи, которые лежат в основе всей атомной физики: атомы, лучи, кванты.
АТОМЫ
Итак, что такое квантовая механика? Квантовая механика — это наука о строении и свойствах атомных объектов и явлений.
В этом определении все верно, и тем не менее бесполезность его очевидна, пока мы не объясним понятий, которые в него входят. Действительно: что, например, означают слова «свойства атомных объектов», то есть атомов?
Если речь идет, скажем, о спелом арбузе, такого вопроса не возникает, — свойства его вполне определяются нашими пятью чувствами: он круглый, тяжелый, сочный, пахнет свежестью и с хрустом раскалывается под ножом. Но как быть с атомами (из которых, кстати, этот арбуз состоит)? Ведь непосредственно их нельзя ни увидеть, ни потрогать. Это не означает, что атомов вообще нет, а просто свидетельствует о том, что свойства их совсем другие, чем свойства целого арбуза.
Сейчас мало осталось людей, для которых реальность атомов менее очевидна, чем движение Земли вокруг Солнца. Почти у каждого с этим понятием связано интуитивное представление о чем-то маленьком и неделимом. И все же, какой смысл вкладывает в понятие «атом» нынешняя физика? Как это понятие возникло, что понимали под ним древние, как оно потом развивалось и почему только квантовая механика наполнила реальным содержанием эту умозрительную схему?
Творцом идеи атома принято считать Демокрита, хотя история упоминает также учителя его Левкиппа и — менее уверенно — древнеиндийского философа Канаду, который жил незадолго до нашей эры и учил примерно тому же. («Канада» в переводе с санскрита означает «пожиратель атомов».) По мнению Канады, бесконечная делимость материи — абсурд, поскольку в этом случае горчичное зерно равно горе, ибо «...бесконечное всегда равно, бесконечному». Мельчайшая частичка в природе, учил Канада, — это пылинка в солнечном луче; она состоит из шести атомов, из которых каждые два соединены попарно «волею бога или еще чем-либо».
О самом Демокрите мы знаем мало. Известно, что родился он в Абдере на фракийском берегу Средиземного моря: кроме Левкиппа, учился у халдеев и персидских магов, много путешествовал и много знал; прожил около ста лет и в 370 году до н. э. был похоронен за общественный счет гражданами родного города, которые его глубоко почитали. Последующие поколения художников изображали Демокрита высоким, с короткой бородой, в белом хитоне и в сандалиях на босу ногу.
Легенда рассказывает, что однажды Демокрит сидел на камне у моря, держал в руке яблоко и размышлял: «Если я сейчас это яблоко разрежу пополам, у меня останется половина яблока; если я затем эту половину снова разрежу на две части, остается четверть яблока;. но если я и дальше буду продолжать такое деление, всегда ли у меня в руке будет оставаться 1/8, 1/16 и т. д. часть яблока? Или же в какой-то момент очередное деление приведет к тому, что оставшаяся часть уже не будет обладать свойствами яблока?» Впоследствии оказалось, что сомнение Демокрита (как почти всякое бескорыстное сомнение) содержало долю истины. По зрелом размышлении философ пришел к выводу, что предел такого деления существует, и назвал эту последнюю, уже неделимую, частицу атомом, а свои умозаключения изложил в книге «Великий диакосмос». Послушайте, это написано более двух тысяч лет назад!
«Начало вселенной — атомы и пустота, все же остальное существует лишь в мнении. Миров бесчисленное множество, и они имеют начало и конец во времени. И ничто не возникает из небытия, не разрешается в небытие. И атомы бесчисленны по величине и по множеству, носятся же они во вселенной, кружась в вихре, и таким образом рождается все сложное: огонь, вода, воздух земля. Дело в том, что последние суть соединения некоторых атомов. Атомы же не поддаются никакому воздействию и неизменяемы вследствие твердости».

Демокрит
Доказать эти утверждения Демокрит не мог - он предлагал поверить на слово. Но ему не поверили, и не поверил прежде всего Аристотель, его великий современник. Когда умер Демокрит, Аристотелю, будущему учителю Александра Македонского, было 14 лет. В расцвете сил он был худощав, невысок ростом, изыскан, а уважение к нему переходило часто все разумные границы. Конечно, для этого были основания: ведь он владел всеми знаниями той эпохи.
Аристотель учил обратному: процесс деления яблока можно продолжить бесконечно, по крайней мере в принципе. Это учение стало господствующим, Демокрита забыли на многие века, а его сочинения тщательно уничтожались.
Бессмысленно винить древних за такой выбор — для них обе системы были равно разумны и приемлемы: цель своей науки они видели не в практических применениях (они их стыдились), а в том, чтобы с помощью умозрения достигнуть того чувства гармонии мира, которое сообщает человеку всякая законченная философия.
Чтобы освободиться от заблуждений великого авторитета, потребовались две тысячи лет. В XVII веке впервые возникла наука физика и вскоре вытеснила древнюю натуральную философию. Эта новая наука опиралась не на чистое умозрение, а на опыт и математику. Окружающую природу стали изучать: не просто наблюдать, а ставить сознательные опыты для проверки гипотез и записывать результаты этой проверки в виде чисел. Идея Аристотеля не выдержала такого испытания, а гипотеза Демокрита выдержала, хотя, как мы увидим в дальнейшем, от ее первоначального вида почти ничего не осталось.
После двадцати веков забвения идею об атомах возродил к жизни французский философ и просветитель Пьер Гассенди (1592—1655) и за это подвергся гонениям церкви: традиции средневековья преследовали не только гипотезы, но и строгие факты науки, если они противоречили общепризнанным догматам. Тем не менее атомную гипотезу приняли все передовые ученые того времени. Даже Ньютон, с его знаменитым девизом «Гипотез не строю», поверил в нее и изложил по-своему в конце третьего тома «Оптики».
Однако до тех пор, пока гипотезу об атомах не подтвердили опытом, она оставалась, несмотря на всю свою привлекательность, только гипотезой.
Первое наглядное доказательство тому, что прав Демокрит, а не Аристотель, обнаружил шотландский ботаник Роберт Браун (1773—1858). В 1827 году это был уже немолодой директор ботанического отдела Британского музея. В юности он провел четыре года в экспедициях по Австралии и привез оттуда около 4 тысяч видов растений. Двадцать лет спустя он все еще продолжал изучать коллекции экспедиции. Летом 1827 года Браун обратил внимание на то, что мельчайшая пыльца растений произвольно двигается в воде под действием неизвестной силы. Он тут же опубликовал статью, заглавие которой очень характерно для той неторопливой эпохи: «Краткий отчет о микроскопических наблюдениях, проделанных в июне, июле и августе 1827 года над частицами, содержащимися в пыльце растений; и о существовании активных молекул в органических и неорганических телах».
Сначала его опыт вызвал недоумение. Это недоумение усугубил сам же Браун, пытаясь объяснить явление некой «живой силой», которая якобы присуща органическим молекулам. Естественно, такое прямолинейное объяснение «брауновского движения» не удовлетворило ученых, и они предприняли новые попытки для его изучения. Среди них особенно много сделали голландец Карбонэль (1880) и француз Гун (1888). Они поставили тщательные опыты и выяснили, что брауновское движение не зависит от внешних воздействий: времени года и суток, добавления солей, вида пыльцы и «...наблюдается одинаково хорошо ночью в деревне и днем вблизи многолюдной улицы, где проезжают тяжелые экипажи».
Надо сказать, что первое время странное движение не обратило на себя должного внимания. Большинство физиков о нем вообще не знало, а те, кто знал, считали его неинтересным, полагая, что это явление аналогично движению пылинок в солнечном луче. Лишь сорок лет спустя, вероятно, впервые оформилась та мысль, что видимые в микроскоп беспорядочные движения пыльцы растений вызваны случайными толчками маленьких, невидимых частиц жидкости. После работ Гун в этом убедились почти все. и гипотеза об атомах приобрела множество последователей.

Атомы
Конечно, и до Брауна немало людей твердо верили, что все тела построены из атомов. Для них некоторые свойства атомов были очевидны уже без дальнейших исследований. В самом деле, все тела в природе, несмотря на огромные различия между собой, имеют вес и размеры. Очевидно, у их атомов также должны быть и вес и размеры. Именно эти их свойства положил в основу своих рассуждений Джон Дальтон (1766—1844) — скромный учитель математики и натуральной философии в городе Манчестере и великий ученый, определивший развитие химии примерно на сто лет.
У сторонников атомистики сразу же возникал вопрос: а не означает ли многообразие тел такого же многообразия атомов, как утверждал Демокрит? Оказалось, это неверно. Джон Дальтон, подробно исследуя химические реакции, в 1808 году впервые четко сформулировал понятие о химическом элементе: элемент — это вещество, которое состоит из атомов одного типа.
Выяснилось, что элементов не так уж много: в то время их знали около 40 (сейчас 104). Все остальные вещества построены из молекул — разнообразных сочетаний атомов. Сами атомы элементов также различаются между собой. Одно из таких различий нашли довольно быстро: им оказалась масса атома. Приняв за единицу атомный вес легчайшего газа — водорода, удалось через него выразить атомный вес остальных элементов. В этих единицах атомный вес кислорода равен 16, железа — 56 и т. д. Так з науку об атоме впервые проникли числа — событие важности необычайной.
Однако по-прежнему об абсолютных размерах и массах атомов ничего не было известно.
Одна из первых научных попыток оценить величину атомов принадлежит Михаилу Васильевичу Ломоносову (1711—1765). В 1742 году он заметил, что искусные ювелиры могут раскатать лист золота до толщины в одну десятитысячную долю сантиметра (10-4 см), и, значит, атомы золота никак не могут превышать этой величины. В 1777 году Бенджамен Франклин (1706—1790) заметил, что ложка масла (ее объем равен примерно 5 см3), вылитого на поверхность спокойной воды, растекается по ней на площади в 0,2 гектара, то есть 2 тыс. кв. м или 2 • 107 см2.
Очевидно, что диаметр молекулы в этом случае
не может превышать величину d = (5 см3)/(2 • 107 см2) = 2,5 • 10-7 (то есть две десятимиллионные доли сантиметра).
Однако первой удавшейся попыткой оценить размер и массу атомов следует считать работу преподавателя физики Венского университета Иозефа Лошмидта (1821—1895). В 1865 году он нашел, что размеры всех атомов примерно одинаковы и равны 10-8 см, а вес атома водорода составляет всего 10-24 г.
Впервые мы встречаемся здесь с такими малыми величинами, и у нас просто нет необходимых навыков, чтобы их осмыслить. Самое большее, на что мы способны, это сказать: тонкий как волос, или легкий как пух. Но толщина волоса (10-2 см) в миллион раз больше самого большого атома, а пуховая подушка — это уже нечто весомое и вполне реальное. Чтобы хоть как-то заполнить провал между здравым смыслом и малостью этих чисел, обычно все же прибегают к сравнению.
Если взять «атом арбуза», с упоминания о котором мы начали рассказ, и вишню диаметром в 1 см и одновременно их увеличивать, то в тот момент, когда вишня станет величиной с земной шар, «атом арбуза» начнет походить — и весом и величиной — на хороший арбуз.
Однако относительная ценность таких сравнений, по-видимому, весьма невелика, поскольку для столь малых объектов само понятие размера теряет свой первичный смысл Поэтому лучше с самого начала оставить попытки представить себе подобные числа наглядно. Несмотря на свою чрезвычайную малость, числа эти не произвольны: важно понимать, что именно такие малые диаметры и массы нужно приписать атомам, чтобы свойства веществ, которые из этих атомов состоят, оказались именно такими, какими мы их наблюдаем в природе.
Лошмидт получил эти числа, изучая взаимную диффузию газов, то есть их способность смешиваться при соприкосновении. (С этим явлением все мы хорошо знакомы, хотя обычно и не вспоминаем о нем, когда нас вдруг остановит запах скошенной травы.) Лошмидт использовал при этом молекулярно-кинетическую гипотезу — предположение, что газы состоят не просто из молекул, но из движущихся молекул. С помощью формул кинетической теории газов он установил также среднее расстояние между молекулами в газе: оно оказалось примерно в 10 раз больше диаметра атомов.
Если газ превратить в жидкость, то его объем уменьшится приблизительно в тысячу раз, а значит, расстояния между атомами уменьшатся в 10 раз. Это означает, что в жидкости и в твердом теле атомы прижаты вплотную друг к другу. Вместе с тем они не перестают двигаться — просто их движение теперь стеснено и подчиняется другим законам, чем законы движения молекул газа.
ЛУЧИ
Железо, как и всякое вещество, состоит из атомов. Если один конец железного лома сунуть в печь, он, разумеется, начнет нагреваться. С точки зрения кинетической теории это означает, что атомы железа начнут двигаться быстрее (это можно обнаружить, коснувшись пальцами другого конца лома). Итак, теплота есть энергия движущихся атомов. Однако это далеко не все.
Нагревая лом, мы наблюдаем поразительное явление: с повышением температуры в печи постепенно меняется цвет нагретого железа: от вишнево-красного до ослепительно белого. Причем к лому теперь нельзя не только прикоснуться, но и просто подойти близко. Последнее уже непонятно, если пользоваться только представлением о движении атомов; действительно, мы не касались лома, атомы железа не ударялись о нашу руку — почему же нам стало жарко?
Здесь мы впервые сталкиваемся с положением, о котором предупреждали в самом начале. Мы должны ввести новое понятие, которое на первый взгляд никак не связано с идеей атома. Это понятие — излучение.
Мы говорим: лучи солнца осветили поляну. Значит, свет — это излучение. Но мы говорим также: греться в лучах солнца. Следовательно, и тепло может распространяться в виде лучей. Вообще с излучением мы имеем дело постоянно: когда сидим у костра, смотрим на закат, вращаем ручку настройки приемника или же делаем рентгеновский снимок грудной клетки. Все виды излучений: тепло, свет, радиоволны и рентгеновы лучи — различные проявления одного и того же электромагнитного излучения. Однако мы все-таки различаем виды излучений не только качественно и субъективно, но и строго количественно. По какому признаку? У электромагнитного излучения их много, но нам особенно важен сейчас один — его волновая природа.
Вероятно, в тысяче и одном учебнике свойства волны объяснены лучше и подробнее, чем мы это сделаем сейчас. Однако мы все-таки напомним их по той же самой причине, по которой даже в солидные академические словари иностранных слов помещают вполне понятные обиходные слова.
«Волна»—одно из самых необходимых слов физики.
Каждый представляет ее себе по-разному: один сразу же видит волны от брошенного в пруд камня, другой — синусоиду. Поскольку синусоиду рисовать проще — воспользуемся ею. У этой схематической волны четыре свойства: амплитуда А, длина волны — λ, частота ν и скорость распространения v.
Амплитуда волны — это наибольшая ее высота. Что такое длина волны — понятно из рисунка. А скорость распространения, по-видимому, особых пояснений не требует. Чтобы выяснить, что такое частота, проследим за движением волны в течение одной секунды.
За это время она пройдет расстояние v сантиметров (то есть ее скорость равна v см/сек). Подсчитав, сколько длин волн уместилось на этом отрезке, мы найдем частоту волны (или излучения): ν = v/λ.
Важнейшее свойство волн — их способность интерферировать. В чем его суть?
Допустите такую возможность: вы с силой бросаете горох в стену так, что он довольно далеко от нее отскакивает. Пусть вам удалось бросать его равномерно, скажем, так, чтобы на один квадратный сантиметр стены в 1 сек. попадало 8 горошин. Теперь мысленно в любом месте между вами и стеной выберите площадку в 1 см2 и сосчитайте число горошин, пролетающих через нее в обе стороны. Ясно, что оно всегда будет равно 16.
А что будет, если от стены отразится волна?
Рассмотрим внимательно рисунок на следующей странице: вначале волна беспрепятственно распространяется вправо (А); затем она достигает стены и отражается (Б); но мы увидим не две отдельные волны, а результат сложения обеих волн: прямой и отраженной. Результат зависит от того, как волна соприкоснулась со стеной (В). Иногда она падает так неудачно, что полностью сама себя гасит (Г, Д). Именно такая способность волны гасить саму себя называется интерференцией. По этому признаку волну всегда можно безошибочно отличить от потока частиц.
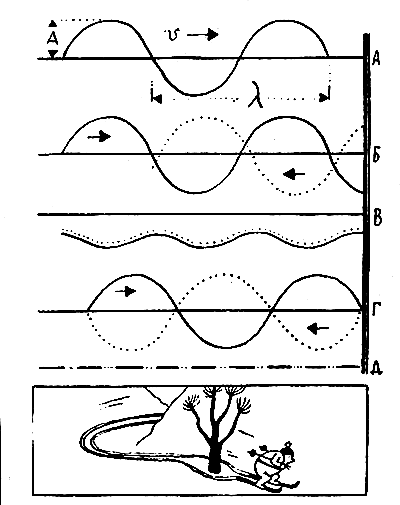
Длины волн
Еще одно свойство волны, которое отличает ее от частиц, — дифракция, или, говоря попросту, способность волны загибать за угол, к чему частица явно не способна. (Отметим только, что размеры препятствия должны быть сравнимы с длиной волны. И еще: если препятствие невелико, то благодаря дифракции волна может разделиться на две, обойти его с двух сторон и, складываясь снова, погасить себя точно так же, как при сложении прямой и отраженной волны.)
Именно таким способом, обнаружив интерференцию и дифракцию у рентгеновского и других видов излучения, установили, что все они волны, только разной длины. Длина волны излучения и есть тот основной признак, по которому мы различаем виды электромагнитного излучения количественно.
Наибольшая длина у радиоволн: от нескольких километров до нескольких сантиметров.
У тепловых лучей она короче — от 1 см до 10-2см.
Еще короче волны видимого света, примерно 4 • 105 — 8 • 10-5 см.
Самые короткие волны у рентгеновых лучей — 10-7-10-9 см.
Все эти виды излучения распространяются с одной и той же скоростью — со скоростью света с = 3 • 1010 см/сек.
Отсюда по формуле ν = c/λ очень просто вычислить частоту каждого вида излучения. Очевидно, для рентгеновых лучей она будет наибольшей, а для радиоволн — наименьшей.
Очень важно отдавать себе отчет в том, что, конечно, любое излучение — это не синусоида, изображенная на рисунке, а физический процесс, основные характеристики которого (например, периодичность), по счастью, можно выразить на языке таких простых моделей.
У каждого вида излучения свои особенности. Сосредоточимся пока на том его виде, который для нас наиболее важен и привычен, — на солнечном излучении. А поскольку оно подчиняется тем же законам, что и любой вид излучения, то в дальнейшем это поможет нам понять законы теплового излучения, которое оказалось столь важным в истории квантовой механики.
Когда вы греетесь на солнце, вы, наверное, не задумываетесь над тем, из каких волн состоят его лучи. Иногда, правда, вы спрашиваете себя, отчего в горах бывают солнечные ожоги и почему нельзя загореть вече- . ром. Исаак Ньютон (1643—1727) жил в Англии, где солнца не так уж много, но все-таки он задумался над тем, Из Чего состоит солнечный свет. Вслед за пражским профессором медицины Маркусом Марци он поставил опыт, знакомый теперь каждому школьнику. Пропустив j луч солнца сквозь призму, он обнаружил за ней на стене радугу — спектр солнечного луча.
Каждому цвету радуги-спектра соответствует своя волна солнечного излучения: самая длинная у красного цвета — 7 • 10-5 см; у зеленого — 5 • 10-5; у фиолетового — 4 • 10-5. Кроме видимых лучей, в солнечном спектре есть, конечно, и другие, в частности инфракрасные лучи (их длины волн еще больше, чем у красных) и ультрафиолетовые (их волны короче фиолетовых). Следовательно, частота ультрафиолетовых лучей наибольшая, а инфракрасных — наименьшая.
Относительная яркость различных цветов в спектре излучения неодинакова и зависит от температуры излучающего тела: например, в солнечном излучении больше всего желтых лучей. Таким образом, спектр любого излучения показывает, во-первых, какие лучи в нем есть и, во-вторых, сколько их там.
Проходя через атмосферу Земли, солнечный луч изменяет свой спектральный состав, потому что разные лучи солнечного спектра поглощаются атмосферой неодинаково, в частности сильнее всего ультрафиолетовые лучи. На горе слой воздуха меньше, доля ультрафиолетовых лучей больше, и потому обгореть там можно быстрее, чем в долине.
И хотя сам по себе этот факт хорошо известен, мы все-таки напомнили эту важную для дальнейшего деталь: причина солнечных ожогов — ультрафиолетовые лучи, именно они, а не зеленые или красные. Но чтобы обжечь, нужно, во всяком случае, затратить какую-то энергию. Следовательно, наибольшую энергию несут с собой волны наибольшей частоты — ультрафиолетовые, а не инфракрасные (хотя именно они и называются тепловыми). Это очень важный результат.
Итак, всякое тело состоит из атомов, которые мы пока представляем себе как шарики диаметром 10-8 см и разного веса: от 10-24 до 20-22 г. Они очень быстро движутся, колеблются и сталкиваются между собой, причем скорость их движения увеличивается с ростом температуры тела. Это тепловое движение атомов приводит к совершенно новому явлению: к тепловому излучению, свойства которого нам пока неизвестны.
Чтобы узнать их, возвратимся к железному лому, который греется в печи. Чем горячее печь, тем больше тепла излучает лом. Конечно, этот факт знали всегда, но только Джозеф Стефан (1835—1893) в 1879 году эмпирически и Людвиг Эдуард Больцман (1844—1906) в 1884 году теоретически установили количественный закон. Оказалось, что с повышением температуры общее количество излучаемого тепла растет очень быстро — как четвертая степень абсолютной температуры тела.
А что, если в печь вместо лома положить булыжник, как делалось раньше в русских банях? Будет ли его энергия излучения отличаться от излучения железного лома? В 1859 году Густав Роберт Кирхгоф доказал, что не будет, если температура печи в обоих случаях одинакова. Он доказал даже нечто большее, но чтобы понять это нечто, нужно прервать рассказ и более пристально посмотреть на поток излучения, который исходит от нагретого тела.
Так же, как и солнечный свет, этот поток неоднороден. Любое тепловое излучение, во-первых, состоит из лучей различной длины волны, и, во-вторых, их вклад в общий поток излучения различен. Если обе эти характеристики мы знаем, то можем утверждать, что нам известен спектральный состав излучения.
Чтобы подчеркнуть тот факт, что доля излучения с частотой ν в общем потоке излучения зависит от температуры Т, обычно пишут такую формулу: U=U (ν, Т).
Конечно, если мы будем менять температуру тела, то спектральный состав его теплового излучения также будет меняться. Количественные законы этого изменения установил в 1893 году Вильгельм Вин (1864—1928).
Но даже при одной и той же температуре различные тела излучают по-разному. В этом нетрудно убедиться, если нагревать в темноте одновременно, например, стальной и каменный шары. Вскоре выяснили, однако, что если вместо сплошных шаров нагревать полые, а излучение наблюдать через небольшое отверстие в их стенках, то спектральный состав этого излучения уже не зависит от вещества шара. Такой спектр назвали спектром абсолютно черного тела.
Происхождение этого несколько необычного названия легко понять. Представьте себе, что вы не нагреваете шар, а, наоборот, освещаете его снаружи. Вы всегда увидите перед собой черное отверстие независимо от материала шара. Потому что все лучи, попавшие внутрь полости, многократно там отражаются и почти не выходят наружу.
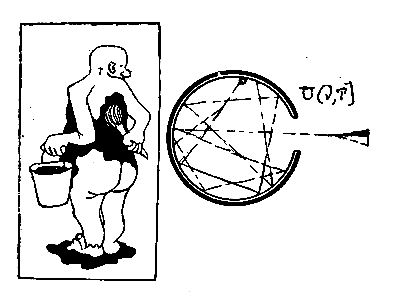
Лучи
Реально существующий пример такого абсолютно черного тела — обычная или, еще лучше, мартеновская печь. Кстати, если вы смотрели когда-либо внутрь мартеновской печи, то, вероятно, обратили внимание на интересное явление: из ее отверстия льется ровный свет, который не позволяет рассмотреть детали предметов, расположенных внутри печи. Наши знания об излучении позволяют нам теперь понять и этот факт.
Два равных по величине шара, каменный и стальной, на солнце очень просто различить — слишком неодинаково они блестят: стальной шар отражает гораздо больше лучей, чем каменный. Если теперь эти шары нагреть в темноте, то нетрудно проверить, что каменный шар излучает больше, чем стальной. (Кстати, это одна из причин, почему в банях выгоднее раскалять булыжники, а не стальные болванки.)
Если эти шары бросить в мартеновскую печь, туда, где они не только нагреваются и излучают сами, но также поглощают и отражают излучение других тел, то мы увидим (разумеется, если взглянем в печь раньше, чем шары расплавятся) два совершенно одинаковых шара. Почему? Да потому, что если каменный шар больше излучает «своих» лучей, то он больше и поглощает «чужих», а стальной меньше излучает «своих» лучей, но зато больше отражает «чужих». Поэтому общий поток лучей («своих» и «чужих») от обоих "шаров одинаков; и поэтому их нельзя отличить не только друг от друга, но даже и от стенок печи, в которой они лежат.
Именно этот строгий закон был установлен Кирхгофом в 1759 году: отношение излучательной способности тел к их поглощательной способности есть универсальная функция: U=U (ν, Т), независимая от природы тел. В спектральной функции U=U (ν, Т) (ее называют и так) заключена почти вся информация о свойствах теплового излучения. В частности, цвет нагретого тела определяют те волны, которых излучается больше всего.
Важность функции U = U (ν, Т) поняли сразу же во времена Кирхгофа, но в течение 40 лет не удавалось найти для нее формулу, которая бы правильно описывала все эксперименты по тепловому излучению. Однако эти попытки никогда не прекращались: по-видимому, поиски абсолютного всегда привлекательны для человеческого ума.
В нашем рассказе мы подошли к порогу переворота, который совершил в физике Макс Планк (1858—1947). Но прежде чем объяснить его суть, еще раз отметим одну особенность теплового излучения, о которой мы однажды упоминали: изменение цвета тел при нагревании.

Макс Планк
Пока температура тела невысока, оно излучает, но не светится, то есть оно испускает только тепловые и инфракрасные волны, невидимые для глаза. При повышении температуры тело начинает светиться: сначала красным цветом, затем оранжевым, желтым и т. д. Например, при 6 тысячах градусов Цельсия больше всего излучается желтых лучей. Кстати, по этому признаку установили, что именно такова температура поверхности Солнца.
Обратите внимание: в случае с солнечным ожогом излучение отдавало тем большую энергию, чем больше его частота. А в данном случае? Чем большую энергию мы затратили на нагревание тела, тем больше частота излучаемых волн. Значит, существует какая-то зависимость между частотой и энергией излучения.
КВАНТЫ
В конце прошлого века Макс Планк искал универсальную формулу для спектра абсолютно черного тела. Как он должен был при этом рассуждать? Тепловое излучение не только порождается движением атомов, но и само воздействует на них, так как несет с собой энергию. В результате такого взаимовлияния внутри абсолютно черного тела устанавливается тепловое равновесие: сколько тепла атомы получают извне, столько же энергии от них уносит излучение. Из кинетической теории материи он знал, что средняя энергия колебаний атомов Екал пропорциональна абсолютной температуре Т: Екол = k•T, где k = 1,38 • 1016 эрг/град — множитель пропорциональности, который называется постоянной Больцмана.
Теперь вспомните: энергия излучения растет с его частотой. Знал это, конечно, и Планк. Но как растет? Он предположил простейшее: энергия излучения Еизлпропорциональна его частоте: Еизл = h • ν, где h — другой множитель пропорциональности. (Мысль эта настолько проста, что ее нельзя доказывать и объяснять через более простые понятия. Однако гениальные мысли отмечает именно такая классическая простота.) Предположив это, Макс Планк угадал формулу для спектральной функции U = U (ν, Т). Да, угадал. Но не надо думать, что все было так уж просто, над своей формулой Планк бился два года.
19 октября 1900 года происходило очередное заседание Немецкого физического общества, на котором экспериментаторы Рубенс и Курлбаум докладывали о новых, более точных измерениях спектра абсолютно черного тела. После доклада состоялась дискуссия, в ходе которой экспериментаторы сетовали, что ни одна из теорий не может объяснить их результаты. Планк предложил им воспользоваться своей формулой. В ту же ночь Рубенс сравнил свои измерения с формулой Планка и убедился, что она правильно, до мельчайших подробностей описывает спектр абсолютно черного тела. Наутро он сообщил об этом своему коллеге и близкому другу Планку и поздравил его с успехом.
Однако Планк был теоретик и потому ценил не только окончательные результаты теорий, но и внутреннее их совершенство. К тому же он не знал еще, что открыл новый закон природы, и считал, что его можно вывести из ранее известных. Поэтому он стремился теоретически обосновать закон излучения, исходя из простых посылок кинетической теории материи и термодинамики. Последовало два месяца непрерывной работы и предельного напряжения сил. Ему это удалось. Но какой ценой!
В процессе вычислений он вынужден был предположить, что излучение испускается порциями (или квантами), величина которых определяется как раз той же формулой Е = h • ν, которую он незадолго перед этим угадал. В этом — и только в этом — случае удавалось получить правильную формулу для спектра излучения.
Соотношение Е = h • ν нельзя доказать логически, как нельзя обосновать закон всемирного тяготения. Они есть — так устроен мир. Более того, только приняв их и с помощью их можно объяснить другие явления природы. И спектр абсолютно черного тела — тоже.
Формально предположение Планка было предельно ясным и простым но, по существу, противоречило всему прежнему опыту физики и годами воспитанной интуиции. Вспомните, мы много раз подчеркивали, что излучение — это волновой процесс. А если так, то энергия в этом процессе должна передаваться непрерывно, а не порциями — квантами. Это неустранимое противоречие Планк сознавал как никто другой. Когда он вывел свою знаменитую формулу, ему было 42 года, но почти всю остальную жизнь он страдал от логического несовершенства им же созданной теории. У последующих поколения физиков это чувство притупилось: они уже знали готовый результат и научились мыслить по-новому.
Но Планк был воспитан на традициях классической физики и целиком принадлежал ее строгому неторопливому миру. А вышло так: разрешив многолетнюю загадку в теории излучения, он тем самым нарушил логическую стройность всей классической физики. «Не слишком ли дорогой ценой достигнуто решение этой, в сущности, очень частной проблемы?» Для Макса Планка это было большим потрясением. Впоследствии, в докладе, который Планк произнес по случаю вручения ему Нобелевской премии, он вспоминал, что для него признание реальности квантов было равносильно «...нарушению непрерывности всех причинных связей».

Кванты
Только значительно позже, в 1927 году, новая наука — квантовая механика — объяснила, что противоречия здесь нет. Но до этого времени еще далеко.
14 декабря 1900 года в зале заседаний Немецкого физического общества родилась новая наука — учение о квантах. Сухо и обстоятельно ординарный профессор физики Макс Карл Эрнст Людвиг Планк прочел перед небольшой аудиторией сугубо специальный доклад: «К теории закона распределения энергии в нормальном спектре».
В тот день мало было людей, которые поняли величие момента: плохая погода или логические противоречия теории, вероятно, занимали аудиторию больше. Признание пришло потом. И позже осмыслили значение постоянной Планка h для всего атомного мира. Она оказалась очень маленькой: h = 6,62 • 10-27 эрг•сек, но она открыла дверь в мир атомных явлений. И всегда, когда мы из мира привычного и классического хотим перейти в мир необычный и квантовый, мы должны пройти через эту узкую дверь.
ВОКРУГ КВАНТА
ЯБЛОКО ДЕМОКРИТА
Мы пока очень мало знаем об атомах, но даже этих знаний достаточно, чтобы решить задачу Демокрита: как долго придется последовательно делить яблоко, чтобы добраться до его «атома»?
Предположим, что у Демокрита в руке было большое яблоко — сантиметров десять в диаметре. Тогда объем его равен примерно
V=103 см3 и при каждом делении уменьшается вдвое, так что после n-го деленияя его объем Vn равен:
Vn = V/22 = 103/100,3•n = 103-0,3•n.
Согласно оценке Лошмидта объем атома равен примерно (10-8 см)3 = 10-24 см3. Деление закончится, когда объем Vn станет равным объему атома, то есть при условии: 103-0,3n = 10-24.
Отсюда легко найти, что n=90, то есть уже на 90 шагу Демокрит достиг бы своей цели. Не так уж много, не правда ли?
Если даже учесть, что он при этом размышлял и потому делил яблоко не торопясь, то и тогда, ему хватило бы получаса.
ИСААК НЬЮТОН ОБ АТОМАХ
«Мне кажется вероятным, что бог вначале создал материю в виде сплошных, массивных, твердых, непроницаемых, движущихся частиц таких размеров и форм и с такими другими свойствами и в таких пропорциях к пространству, которые наилучшим образом служат той цели, для которой он их создал, и что эти простейшие частицы, будучи твердыми, несравненно прочнее, чем любые другие тела, составленные из них; даже настолько прочны, что никогда не изнашиваются и не разбиваются на куски; никакие обычные силы не в состоянии разделить то, что бог создал сам в первый день творения...»
«Мне кажется очевидным, что эти частицы имеют не только свойство инерции вместе с такими пассивными законами движения, которые естественно следуют из этих сил, но что они движутся согласно определенным действующим принципам, подобным гравитации, и которые являются причиной возбуждения и сцепления тел. Эти принципы я рассматриваю не как оккультные качества, предположенные для того, чтобы вывести результаты, исходя из специфических форм вещей, но как общие законы природы, которым обязано само существование этих вещей; их достоверность очевидна нам через явления, хотя их причины пока что не открыты. Явны только качества, а их причины неизвестны».
ПЛАНК О КВАНТЕ
В Шведской академии наук в Стокгольме Макс Планк при вручении ему Нобелевской премии 2 июня 1920 года произнес речь «Возникновение и постепенное развитие теории квантов». Приведем несколько выдержек из нее.
«Крушение всех попыток перебросить мост через возникшую пропасть вскоре уничтожило все сомнения: или квант действия был фиктивной величиной — тогда весь вывод закона излучения был принципиально иллюзорным и представлял просто лишенную содержания игру в формулы, или при выводе этого закона в основу была положена правильная физическая мысль — тогда квант действия должен был играть в физике фундаментальную роль, тогда появление его возвещало нечто совершенно новое, дотоле неслыханное, что, казалось, требовало преобразования самой основы нашего физического мышления, покоившегося со времен обоснования анализа бесконечно малых Ньютоном и Лейбницем на предположении о непрерывности всех причинных связей...»
«...То, что сегодня кажется нам непонятным, когда-нибудь будет казаться, с более высокой точки зрения, особенно простым и гармоничным. Но прежде чем эта цель будет достигнута, проблема кванта действия не перестанет побуждать и оплодотворять мысль исследователей, и чем большие трудности представятся в ее решении, тем важнее она окажется для расширения и углубления всего нашего физического знания».
Планк прекрасно сознавал значение своего открытия (он говорил сыну: «Сегодня я сделал открытие такое же важное, как Ньютон»), но никогда этого не афишировал. Вероятно, поэтому укоренилось заблуждение, что Планк, «очевидно, не знал, что он делает, когда делал это». Приведенные отрывки из нобелевской речи лишний раз опровергают это заблуждение.
http://www.rostakelag.ru/ услуги грузчиков у нас только профессиональные такелажники.
|
ПОИСК:
|