
ГЛАВА ДЕСЯТАЯ
Игра в «орел-решку» - Стрельба в тире - Дифракция электронов - Волны вероятности - Из чего состоит электронная волна? - Атом - Вероятность и спектры атомов - Причинность и случайность, вероятность и достоверность
Представьте себе, что где-то в поезде между Новосибирском и Красноярском вы познакомились с хорошим человеком. Теперь вообразите, что год спустя вы случайно встречаете его в Москве у кинотеатра «Россия». Как бы вы ни были рады встрече, прежде всего вы удивитесь, потому что знаете по опыту, насколько такое событие маловероятно.
Глава десятая
Мы постоянно употребляем слова «вероятно», «вероятнее всего», «по всей вероятности», «невероятно», не отдавая себе отчета, насколько строго определены понятия, им соответствующие. В науке такое положение недопустимо, поэтому там понятие «вероятность» имеет смысл лишь в, том случае, если мы можем ее вычислить.
Это не всегда возможно. Например, нельзя предсказать вероятность случайной встречи с вашим случайным знакомым в 6 часов вечера 23 октября 1975 года на Главпочтамте города Липецка, хотя заведомо ясно, что эта вероятность не равна нулю. Но поступки людей не случайны, и применять к ним теорию вероятностей нельзя. Поэтому во всех учебниках с завидным постоянством объясняют законы случая на примере бросания монеты.
ИГРА В «ОРЕЛ-РЕШКУ»
Прежде всего заметим: если событие имеет несколько исходов, то полная вероятность произойти хоть какому-то из них равна единице. Поэтому слова «событие произойдет с вероятностью единица» означают, что оно произойдет наверняка.
Отсюда ясно также, что вероятность какого-то одного исхода всегда меньше единицы. В примере с монетой случайное событие — бросание монеты — имеет только два исхода: она может упасть либо гербом вверх, либо гербом вниз. (Мы исключаем неправдоподобно редкие случаи, когда монета при падении останется стоять на ребре.) Если монета сделана без хитростей, то логично предположить, что оба исхода бросания равновероятны. Отсюда сразу же следует, что вероятность выпадания, скажем, герба равна 1/2.
Столь же легко вычислить вероятность выпадания, скажем, 3 очков при бросании игральной кости: очевидно, она равна 1/6.
Число аналогичных примеров каждый легко умножит сам, но все они очень похожи.
Во-первых, каждое последующее событие (бросание монеты) не зависит от предыдущего.
Во-вторых, они строго случайны, то есть мы не знаем (или не можем учесть) всех причин, которые приводят к тому или иному исходу события.
Последнее особенно важно. В самом деле, монета не атом, и ее движение подчиняется хорошо известным законам классической механики. Используя их, мы бы могли заранее предвидеть все детали движения монеты и предсказать, как она упадет: гербом вверх или вниз. Нам под силу даже нарисовать ее траекторию движения. Конечно, это очень трудно: нужно принять во внимание сопротивление воздуха, форму монеты, упругость пола, на который она упадет, и еще много других важных мелочей. И — самое главное — необходимо точно задать начальное положение и импульс монеты.
Однако учесть все мыслимые факторы, влияющие на исход событий, не всегда возможно. Например, в случае с монетой мы никогда не знаем достаточно точно ее начального положения и скорости. А всякое, даже очень небольшое, их нарушение может изменить результат бросания на противоположный. И тогда уже нельзя быть уверенным, что при этом бросании монета упадет гербом вверх. Можно только сказать: вероятность выпадания герба при любом бросании равна 1/2.
Простые примеры, которые мы привели, не объясняют пока, почему так важно понятие вероятности в квантовой механике. Но прежде чем объяснить это, познакомимся хотя бы бегло с основными законами теории вероятностей. Законы случая (несмотря на странное сочетание двух этих слов) такие же строгие, как и всякие другие законы математики. Однако они имеют некоторые непривычные особенности и вполне определенную область применимости.
Например, хотя мы и знаем, что вероятность выпадания герба при бросании монеты равна 1/2, однако предсказать исход одного отдельно взятого бросания мы не в состоянии. Тем не менее мы легко можем проверить, что при большом числе бросаний герб выпадет примерно в половине случаев, и закон этот выполняется тем точнее, чем больше испытаний мы проведем. В этом и состоит главная особенность закона случайных событий: понятие вероятности применимо к отдельному событию, и мы можем вычислить заранее число, которое этому понятию соответствует. Однако измерить это число можно только при многократном повторении однотипных событий.

Игра в «орел-решку»
Очень важно, чтобы события были однотипными, то есть полностью неразличимыми, поскольку только тогда измеренное число — вероятность — можно использовать для оценки каждого отдельного события.
Непривычные особенности законов случая имеют естественное объяснение. В самом деле, бросание монеты — очень непростой процесс. Мы не хотим или не умеем изучать его во всей сложности. Поэтому мы намеренно закрываем глаза на всю его сложность, отказываемся следить за траекторией монеты и хотим знать только конечный результат испытания. Такое пренебрежение к деталям процесса не проходит даром — теперь мы можем достоверно предсказать только усредненный результат многочисленных однотипных испытаний, а для каждого отдельного события мы в состоянии указать лишь вероятный его исход.
Широко бытует заблуждение, что вероятностное описание движения менее полно, чем строго причинное, классическое, с его понятием траектории. С точки зрения классической механики это действительно так. Однако если мы откажемся от части ее жестких требований (например, от знания начальных координат и импульсов), тогда классическое описание бесполезно. На смену ему приходит вероятностное, и в новых условиях оно будет исчерпывающим, поскольку сообщает нам все сведения о системе, которые мы вообще можем узнать о ней с помощью опыта.
СТРЕЛЬБА В ТИРЕ
При игре в «орел-решку» мы Намеренно не хотим, знать начального положения и скорости монеты и целиком полагаемся на волю случая. Несколько другие
желания одолевают нас в тире: там мы всегда стремимся попасть в центр мишени. Но, несмотря на это стремление (довольно сильное), мы никогда заранее не знаем, в какое место мишени попадет каждая из пуль. Попадания группируются в довольно правильный овал, который принято называть «эллипсом рассеяния». От чего он зависит?
Стрельба
Очевидно, чтобы все пули, вылетающие из винтовки, попадали всегда в одну и ту же точку мишени, необходимо, чтобы в момент вылета все они имели одни и те же начальные координаты х и скорости v (или импульсы р). А это возможно лишь в том случае, если вы целитесь безошибочно и, кроме того, заряд пороха во всех патронах всегда в точности одинаков.
Ни то, ни другое обычно недостижимо. Поэтому распределение отверстий от пуль на мишени всегда подчиняется законам случая, и можно говорить лишь о вероятности попадания в «десятку» или «девятку» мишени, но никогда нельзя быть уверенным в этом заранее.
Как и при игре в «орел-решку», эту вероятность можно измерить. Допустим, мы произвели 100 выстрелов и 40 раз попали в «десятку», 30 раз — в «девятку», 15 — в «восьмерку» и так далее — до нуля. Тогда вероятности попадания в «десятку», «девятку», «восьмерку» и т. д. соответственно равны: W(10)=40/100=0,4; W(9)=0,3; W(8)=0,15 и т.д.
Можно даже построить диаграмму, которая как бы показывает внутреннюю структуру эллипса рассеяния.
Если мы возьмем теперь такую же мишень и вновь 100 раз по ней выстрелим, то расположение отверстий на ней будет совсем другим, чем на первой мишени. Но число попаданий в «десятку», «девятку» и т. д. останется примерно тем же самым, а следовательно, и диаграмма эллипса рассеяния также останется без изменения.
Конечно, для разных стрелков диаграммы различны: для опытного стрелка они уже, для неопытного — шире. Но для каждого отдельного стрелка она остается неизменной, так что опытный тренер по одному виду мишени может установить, кому из его учеников она принадлежит.

Стрельба в тире
Из приведенных простых примеров следует, что «законы случая» — это не пустая игра слов. Конечно, каждая отдельно взятая пуля попадет в случайную точку мишени, которую нельзя предсказать заранее. Однако при большом числе выстрелов попадания образуют настолько закономерную картину, что мы воспринимаем ее как достоверную и совершенно забываем о вероятности, лежащей в ее основе.
ДИФРАКЦИЯ ЭЛЕКТРОНОВ
Простой пример со стрельбой напоминает опыты квантовой механики значительно больше, чем это может показаться на первый взгляд. Чтобы убедиться в этом, заменим ружье «электронной пушкой», мишень — фотопластинкой, а между ними поместим тонкую металлическую фольгу.
«Электронная пушка» не шутка, а научный термин, который обозначает устройство для получения пучка электронов примерно такое же, как в телевизионной трубке (или трубке Крукса). Из этого пучка с помощью диафрагм и фокусирующих линз мы можем выделить очень узкий электронный луч, в котором все электроны движутся с одинаковой скоростью.
Теперь направим этот луч через металлическую фольгу на фотопластинку и затем проявим ее. Какое изображение мы на ней увидим? Точку? Эллипс рассеяния, как при стрельбе в тире? Или что-нибудь еще? Ответ нам давно известен: на фотопластинке мы увидим дифракционные кольца, подобные тем, которые изображены на предыдущей странице. Мы можем теперь объяснить даже причину их появления.
В самом деле, мы много раз повторяли, что электрон — это не только частица, но также и волна. И если до сих пор мы еще не привыкли к этому факту, то, во всяком случае, должны были его запомнить. Поэтому сама по себе дифракция электронов не должна нас теперь удивлять: явление дифракции возникает всегда, если через вещество проходит волна. Вопрос не в этом. Волна чего проходит вместе с электроном через фольгу?
По морю гуляют морские волны — они состоят из воды. Космос пронизывают электромагнитные волны — они представляют собой колебания электрического и магнитного полей. Из чего состоит волна электрона, если сам он неделим и не имеет внутренней структуры?
Дифракция электронов
Прежде чем ответить на эти вопросы, поставим опыт с пучком электронов немного по-другому. Станем выпускать электроны по одному (как пули из винтовки) и каждый раз менять фотопластинку за фольгой. После проявления всех фотопластинок мы обнаружим на каждой из них точку — след от упавшего электрона. (Уже один этот факт, если бы не было других доказательств, легко убеждает нас в том, что электрон — все-таки частица.) На первый взгляд черные точки на пластинках расположены совершенно беспорядочно, и, конечно, ни одна из точек ничем не напоминает дифракционную картину. Но если мы сложим все пластинки в одну стопку и посмотрим ее на просвет, то с удивлением обнаружим все те же дифракционные кольца. Стало быть, черные следы от электронов расположены на пластинках не так уж беспорядочно, как может показаться вначале.
Этот простой опыт настолько прост, что может даже обидеть некоторых читателей своей тривиальностью. Однако в свое время именно он убедил последних противников квантовой механики. Конечно, вовсе не обязательно для каждого электрона брать отдельную пластинку, вполне достаточно одной пластинки-мишени, только по-прежнему надо пускать электроны-пули поодиночке.
Как и прежде, мы не можем заранее предсказать, в какую точку пластинки попадет каждый следующий электрон. Это случайное событие. Однако если мы выпустим достаточно много электронов, то получим закономерную дифракционную картину.
С такими явлениями мы уже сталкивались при игре в «орел-решку», при бросании кости, при стрельбе в тире. Отмеченная аналогия приводит к естественному предположению: процесс рассеяния электронов подчиняется законам теории вероятностей. При дальнейшем размышлении и после знакомства с идеями Макса Борна эта догадка сменяется уверенностью.
ВОЛНЫ ВЕРОЯТНОСТИ
Макс Борн (1882—1970) преподавал физику в признанном центре немецкой науки — в Геттингене. Он пристально следил за развитием теории атома и был одним из первых, кто придал квантовым идеям Гейзенберга строгую математическую форму. В начале 1927 года он заинтересовался опытами по дифракции электронов.
Само по себе это явление после работ де Бройля уже не казалось удивительным. Любой физик, взглянув на дифракционную картину, мог бы теперь объяснить ее появление с помощью гипотезы о «волнах материи». Более того, по формуле де Бройля λ = h/m v; он мог вычислить длину этих «волн материи» и на опыте убедиться в правильности своих вычислений. Однако по-прежнему никто не мог объяснить, что он разумеет под словами «волны материи». Пульсацию электрона-шарика? Колебания какого-то эфира? Или вибрацию чего-либо еще более гипотетического? То есть насколько материальны сами «волны материи».
Волны вероятности
Летом 1927 года Макс Борн предположил: «волны материи» — это просто «волны вероятности», которые описывают вероятное поведение отдельного электрона, например вероятность его попадания в определенную точку фотопластинки.
Всякая новая и глубокая идея не имеет логических оснований, хотя нестрогие аналогии, которые к ней привели, можно проследить почти всегда. Поэтому вместо того чтобы доказывать правоту Борна (это невозможно), попытаемся почувствовать естественность его гипотезы. Обратимся снова к игре в «орел-решку» и вспомним причины, которые вынудили нас тогда применить теорию вероятностей. Их три:
полная независимость отдельных бросаний монеты;
полная неразличимость отдельных бросаний;
случайность исхода каждого отдельного бросания, которая проистекает от полного незнания начальных условий каждого опыта, то есть от неопределенности начальной координаты и импульса монеты.
Все эти три условия выполняются в атомных явлениях и, в частности, в опытах по рассеянию электронов. В самом деле:
электроны ведь все-таки частицы, и потому каждый из них рассеивается независимо от других;
кроме того, электроны так бедны свойствами (заряд, масса, спин — и все), что в квантовой механике они неразличимы, а вместе с тем неразличимы и отдельные акты рассеяния;
и наконец, начальные значения координат и импульсов электронов нельзя определить даже в принципе — это запрещено соотношением неопределенностей Гейзенберга δx δp ≥ 1/2h.
В таких условиях бессмысленно искать траекторию каждого электрона. Вместо этого мы должны научиться вычислять вероятность ρ(х) попадания электронов в определенное место х фотопластинки (или, как принято говорить в физике, вычислять функцию распределения ρ(х)).
При игре в «орел-решку» это очень просто: даже без вычислений ясно, что вероятность выпадания «орла» равна 1/2- В квантовой механике дело немного осложняется. Чтобы найти функцию ρ(х), описывающую распределение электронов на фотопластинке, необходимо решить уравнение Шредингера.
Макс Борн утверждал: вероятность ρ(х) найти электрон в точке х равна квадрату волновой функции ρ(x) = |ψ(x)|2
Утверждение Борна легко проверить. В самом деле, разделим дифракционную картину на концентрические круги и пронумеруем их, как мишень в тире. Затем сосчитаем число Nk электронов, попавших в каждое кольцо с радиусом xk, и поделим эти числа на общее число электронов N, попавших на пластинку. Тогда, как и в случае стрелковой мишени, мы получим набор чисел ρ(xk) = Nk/N, которые равны вероятности обнаружить электрон на расстоянии хk от центра мишени. Теперь не трудно нарисовать распределение электронов по пластинке и проследить, как меняется их число при удалении от центра дифракционной картины.
График функции ρ(х) выглядит сложнее, чем диаграмма эллипса рассеяния при стрельбе в тире. Но если вид эллипса нам не под силу предсказать, то функцию ρ(х) мы можем вычислить заранее. Ее вид однозначно определяется законами квантовой механики: несмотря на свою необычность, они все-таки существуют, чего нельзя сказать с уверенностью о законах поведения человека, от которого зависит эллипс рассеяния.
ИЗ ЧЕГО СОСТОИТ ЭЛЕКТРОННАЯ ВОЛНА?
Когда мы стоим на берегу моря, то у нас не возникает сомнений, что на берег набегают волны, а не что-либо другое. И нас не удивляет тот достоверный факт, что все волны состоят из огромного числа частиц — молекул.
Волны вероятности — такая же реальность, как и морские волны. И нас не должно смущать то обстоятельство, что волны эти построены из большого числа отдельных, независимых и случайных событий.
Морской воде присущи и свойства волны, и свойства частиц одновременно. Это нам кажется естественным. И если мы удивлены, обнаружив такие же свойства у вероятности, то наше недоумение, по крайней мере, нелогично.
Когда дует ветер, то в море из беспорядочного скопления отдельных молекул возникают правильные ряды волн. Точно так же, когда мы рассеиваем пучок электронов, то отдельные случайные события — пути электронов — закономерно группируются в единую волну вероятности.
Чтобы убедиться в реальности морских волн, не обязательно попадать в кораблекрушение, но хотя бы поглядеть на море желательно. Чтобы обнаружить волны вероятности, нужны сложные приборы и специальные опыты. Конечно, эти опыты сложнее, чем простой взгляд с прибрежного утеса к горизонту, но ведь нельзя же только на этом основании отрицать само существование вероятностных волн.
Полистав толстые учебники гидродинамики, можно убедиться, что пути молекул, из которых состоит морская волна, ничем не напоминают волновых движений: молекулы движутся по кругам и эллипсам, вверх и вниз и вовсе не участвуют в поступательном движении волны. Они составляют волну, но не следуют за ее движением. Форму этой волны определяют законы гидродинамики.
Из чего состоит электронная волна
Точно так же движение отдельных электронов в атоме вовсе не похоже на те колебания, которым мы уподобили его раньше. Но в целом ненаблюдаемые пути электронов принадлежат единому наблюдаемому ансамблю — волне вероятности. Форму этой волны диктуют законы квантовой механики.
Аналогии такого рода можно продолжать и дальше, но сейчас важнее уяснить другое. Как теперь надо понимать слова «электрон — это волна»? Ведь если это не материальная волна, а волна вероятности, то ее даже нельзя обнаружить в опытах с отдельным электроном. Иногда волновой характер квантовомеханических явлений трактуют как результат некоего мистического взаимодействия большого числа частиц между собой. Это объяснение мотивируют как раз тем, что волновые закономерности атомных явлений вообще нельзя обнаружить, если проводить опыты с отдельно взятой атомной частицей. Ошибка таких рассуждений объясняется элементарным непониманием природы вероятностных законов: вычислить волновую функцию ψ(х) и распределение вероятностей ρ(x) можно для отдельной частицы, но измерить распределение ρ(х) можно только при многократном повторении однотипных испытаний с одинаковыми частицами.
И все же вероятность — это характеристика отдельного события. А потому каждому электрону присущи волновые свойства, хотя мы обнаружить их можем только в пучке электронов. (Точно так же при игре в «орел-решку» вероятность 1/2 выпадения «орла» — это свойство каждого события, но измерить эту вероятность можно лишь при большом числе испытаний.)
Без понятия вероятности современную квантовую механику представить очень трудно. Пожалуй, это главное, чем она отличается от механики классической. Конечно, и классическая физика постоянно использует теорию вероятностей. Например, в кинетической теории газов. Однако там еще можно успокаивать себя в надежде обойтись без теории вероятностей, если удастся научиться решать одновременно очень много уравнений движения молекул газа. Квантовая механика не оставляет такой надежды, ее уравнения принципиально позволяют вычислять только вероятности событий. Тем не менее для атомных явлений это описание будет настолько же полным, насколько исчерпывающе описание классического движения с помощью понятия траектории.
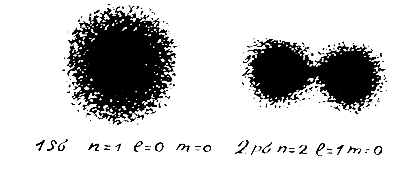
Форма атома 1
Все предыдущие примеры и рассуждения помогают нам понять, что представляет собой электрон вне атома и почему эта частица наделена также свойствами волны. Как же эти свойства — волны и частицы — можно совместить без логических противоречий внутри атома?
АТОМ
Если вы заметили, мы нигде не пытались определить форму атома непосредственно на опыте. Мы ее вычислили из волнового уравнения Шредингера. Мы в нее поверили, поскольку то же самое уравнение позволяет правильно предсказать самые тонкие особенности наблюдаемых спектров атомов. Сейчас эта форма атомов общепризнана, и в предыдущей главе мы даже нарисовали несколько таких форм.
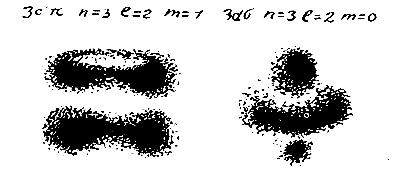
Форма атома 2
Однако если понимать приведенные рисунки атома буквально, то приходится представлять себе электрон как некое заряженное облако, форма которого зависит от степени возбуждения атома. По многим причинам такая картина неудовлетворительна.
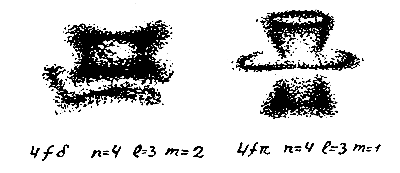
Форма атома 3
Прежде всего электрон — все-таки частица, и убедиться в этом очень просто, наблюдая, например, его следы в камере Вильсона. Кроме того, мы теперь достаточно хорошо знаем, что никаких реальных колебаний и материальных волн в атоме нет. Реальны только волны вероятности. Как это новое знание изменит наши прежние представления об атоме?
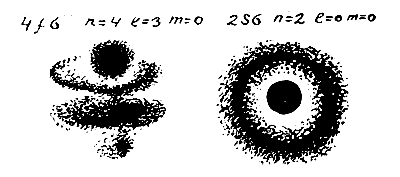
Форма атома 4
Поставим мысленный опыт по определению формы атома водорода. Возьмем, как и прежде, «электронную пушку», но теперь будем обстреливать из нее не фольгу, а отдельно взятый атом водорода. Что мы при этом должны увидеть?
Большинство электронов «прошьет» атом водорода, как снаряд рыхлое облако, не свернув с пути. Но, наконец, один из них, столкнувшись с электроном атома, вырвет его оттуда и при этом сам изменит направление своего движения. Теперь позади атома мы увидим не один, а два электрона: один — из «пушки», другой — из атома. Допустим, что мы так точно измерили их пути, что можем восстановить точку их встречи в атоме. Можем ли мы на этом основании утверждать, что электрон в атоме водорода находился именно в этой точке?
Нет, не можем. Мы не в состоянии даже проверить свое допущение, поскольку атома водорода больше не существует — наше измерение его разрушило.
Этой беде, однако, легко помочь: все атомы водорода неразличимы, и, чтобы повторить опыт, можно взять любой из них. Повторный опыт нас разочарует: мы обнаружим электрон в атоме совсем не там, где ожидали найти его на основании первого измерения.
Третье, пятое, десятое измерения только укрепят нашу уверенность в том, что электрон в атоме не имеет определенного положения: каждый раз мы будем его находить в новом месте. Но если мы возьмем очень много атомов, проведем очень много измерений и при этом всякий раз будем отмечать точкой место электрона в атоме, найденное в каждом отдельном опыте, то в конце концов мы с удивлением обнаружим, что точки эти расположены не беспорядочно, а группируются в уже знакомые нам фигуры, которые мы раньше вычислили из уравнения Шредингера.
Из опытов по дифракции электронов мы уже знаем, как объяснить этот факт. В самом деле, тогда мы не знали, в какое место фотопластинки попадет электрон, теперь мы не знаем, в каком месте атома мы его найдем. Как и прежде, сейчас мы можем указать только вероятность обнаружения электрона в каком-то определенном месте атома.
В одной точке атома эта вероятность больше, в другой — меньше, но в целом распределение вероятностей образует закономерный силуэт, который мы и принимаем за форму атома.
Ничего другого нам не остается. Можно, конечно, возразить, что это не отдельный атом, а некий обобщенный образ многих атомов. Но это будет слабый аргумент: ведь все атомы в одном и том же квантовом состоянии неразличимы между собой. Поэтому точечные картинки, полученные в опыте по рассеянию электронов на многих, но одинаковых атомах, определяют одновременно форму и обобщенного атома, и одного отдельно взятого атома.
Здесь, как и всегда, где работают законы случая, необходимо учитывать их особенности. Для каждого отдельного атома функция ρ(x) указывает лишь распределение вероятностей найти электрон в точке х атома. Именно в этом смысле можно говорить о «вероятной форме отдельного атома». Но картина эта достоверна, поскольку она совершенно однозначна для любой совокупности одинаковых атомов.
Наша теперешняя картина атома бесконечно далека от представлений Демокрита. В сущности, от его представлений почти ничего не осталось.
Но плодотворные заблуждения всегда лучше, чем бесплодная непогрешимость. Не будь их, Колумб никогда бы не открыл Америку.
Сейчас мы достигли предела, который вообще доступен тем, кто пытается проникнуть в глубь атома без формул и уравнений. Тем не менее образ, который мы для себя сформировали, верен во всех деталях. Не пользуясь «математической кухней» квантовой механики, мы не сможем предсказать ни одного атомного явления, однако объяснить кое-что мы теперь в состоянии, если будем использовать новый образ атома грамотно и помнить о его происхождении.
ВЕРОЯТНОСТЬ И СПЕКТРЫ АТОМОВ
Не только форма атома, но и все процессы в нем подчиняются законам теории вероятностей. Имея дело с отдельным атомом, никогда нельзя сказать наверняка, где находится его электрон, куда он попадет в следующий момент и что произойдет при этом с самим атомом.
Однако уравнения квантовой механики всегда позволяют вычислить вероятности всех этих процессов. Вероятностные предсказания можно потом проверить и убедиться, что они достоверны, если провести достаточно много одинаковых испытаний. Даже такие люди, как Резерфорд, далеко не сразу поняли эту особенность атомных процессов.
Он был первым читателем тогда еще рукописной статьи Бора о строении атомов. Ознакомившись с ней, Резерфорд с присущей ему прямотой и резкостью спросил Бора: «А откуда электрон, сидящий на n-й орбите, знает, куда ему надо прыгнуть: на k-ю или на j-ю орбиту?» Тогда, в 1913 году, Бор ничего не смог ответить Резерфорду. И лишь теперь, после работы трех поколении физиков, вопрос прояснился до такой степени, что даже мы в состоянии в нем разобраться.
Электрон вовсе ничего «не знает» заранее - он лишь подчиняется законам квантовой механики. Согласно этим законам для электрона в любом квантовом состоянии (например, в состоянии с квантовым числом n) всегда существует строго определенная вероятность перейти в любое другое состояние (например, в состояние k). Как всегда, вероятность Wnk перехода n ->k — это число, значение которго зависит от выбора пары квантовых состояний n и k. И если мы переберем всевозможные комбинации номеров n и k, то получим квадратную таблицу чисел Wnk. Мы уже знаем, что такая таблица называется матрицей. И матрица эта представляет внутреннее состояние атома.
Только теперь мы можем оценить интуицию Гейзенберга, который, ничего не зная о законах вероятности, управляющих квантовыми процессами в атоме все-таки правильно почувствовал их особенности и ввел свои матрицы. {Xnk} и {Pnk}. Как выяснилось немного позже, через эти матрицы матрица вероятности Wnk выражается довольно просто. А матрицы Гейзенберга, в свою очередь, легко вычислить, решив уравнение Шредингера.
Рассуждения, которые мы только что проследили, несмотря на свою простоту, весьма плодотворны. Например, с их помощью довольно легко можно объяснить, почему в желтом дублете D-линии натрия — линия D2 в два раза интенсивнее, чем линия D1.
Более того, последовательно используя уравнения квантовой механики, можно выяснить и более тонкие особенности строения этих линий, например законы изменения интенсивности внутри их самих. Но все эти радости доступны только специалистам.
ПРИЧИННОСТЬ И СЛУЧАЙНОСТЬ, ВЕРОЯТНОСТЬ И ДОСТОВЕРНОСТЬ
Вероятностная интерпретация квантовой механики очень многим пришлась не по душе и вызвала многочисленные попытки возврата к прежней, классической схеме описания. Это стремление во что бы то ни стало использовать старые знания в новых условиях по-человечески понятно, но ничем не оправдано. Оно напоминает желание отставного солдата осмыслить все многообразие жизни с позиций строевого устава. Безусловно, его возмутит беспорядок на танцплощадке, и довольно трудно будет объяснить ему, что там действуют несколько иные законы, чем на армейском плацу.
Еще не так давно недобросовестные интерпретаторы квантовой механики с подозрительным рвением пытались отменить ее только на том основании, что она не укладывалась в рамки ими же придуманных схем. Они возмущались «свободой воли», которая якобы дарована электрону, шельмовали соотношение неопределенностей и всерьез доказывали, что квантовая механика — бесполезная наука, коль скоро она толкует не о реальных событиях, а об их вероятностях. Те, кто внимательно проследил предыдущие рассуждения, понимают всю вздорность подобных обвинений. Но даже те, кто относится уважительно к теории атома, не всегда четко сознают, как понимать причинность атомных явлений, если каждое из них — случайно; и насколько достоверны ее предсказания, если все они основаны на понятии вероятности.
Причинность и случайность
Житейское понятие причинности: «Всякое явление имеет свою причину» — не требует объяснений, но для науки бесполезно. Причинность в науке требует строгого закона, с помощью которого можно проследить последовательность событий во времени. На языке формул этот закон принимает вид дифференциального уравнения, которое называют уравнением движения. В классической механике такие уравнения — уравнения движения Ньютона — позволяют предсказать траекторию движения частицы.
Именно такая бегло очерченная нами схема объяснения и предсказания явлений природы всегда составляла идеал причинного описания в классической физике. Она не оставляет места для сомнений и кривотолков, и, чтобы подчеркнуть это ее качество в дальнейшем, причинность классической физики назвали детерминизмом.
Такой причинности в атомной физике нет. Но там есть своя — квантовомеханическая причинность и свой закон — уравнение Шредингера. Он даже более могуществен, чем уравнения Ньютона, так как улавливает и выделяет закономерности в хаосе случайных атомных событий. Подобно калейдоскопу, который в случайном сочетании стеклышек позволяет разглядеть фигуры, имеющие смысл и красоту.
Сочетания слов «статистическая причинность», «вероятностная закономерность» с непривычки режут слух своей несовместимостью. («Масляное масло» — плохо, но все же разумно, однако «немасленое масло» — это уж слишком.) Они и в самом деле несовместимы. Но в атомной физике мы вынуждены использовать их одновременно для того, чтобы во всей полноте объяснить особенности квантовых явлений. В действительности никакого логического парадокса здесь нет: понятия «случайность» и «закономерность» — дополнительные понятия. В согласии с принципом дополнительности Бора оба они одновременно и равно необходимы, чтобы определить новое понятие «квантовомеханическая причинность», которая есть нечто большее, чем простая сумма понятий «закономерность» и «случайность». Точно так же, как «атомный объект» всегда нечто более сложное, чем бесхитростная сумма свойств «волны» и «частицы».
При всей логической красоте таких построений привыкнуть к ним и признать их естественными все-таки довольно трудно. Как всегда, в квантовой физике эти логические трудности объясняются особенностями нашего языка и нашего воспитания. Понятия «закономерность» и «случайность», «достоверность» и «вероятность» возникли задолго до квантовой механики, и смысл, который в них обычно вкладывают, не зависит от желания квантовых физиков. По существу, проблема вероятности — это всегда проблема наблюдения: что произойдет, если мы проделаем то-то и то-то.
В классической физике два одинаковых испытания при одинаковых начальных условиях всегда должны приводить к одному и тому же конечному результату. В этом суть классической причинности, или детерминизма. Своеобразие квантовомеханической причинности состоит в том, что даже при неизменных условиях она может указать лишь вероятность отдельного испытания, но зато совершенно достоверно предсказывает общую картину при большом числе тех же самых испытаний.
Можно без конца жонглировать парадоксами «закономерная случайность», «достоверная вероятность», однако это ничего не прибавит к нашим знаниям об атоме. Суть не в этом. Просто нужно понять хотя бы однажды, что вероятностное описание атома — это не результат усреднения пока неизвестных нам атомных моделей (как это было в случае с бросанием монеты). Здесь мы дошли до предела возможностей нынешней науки: пока остается в силе соотношение неопределенностей Гейзенберга, мы принципиально не можем уточнять наши сведения об атомных системах. По существу, нам это и не нужно: все тела в природе состоят из огромного числа атомов, а свойства таких систем квантовая механика предсказывает однозначно и без всякого произвола.
Понятие о вероятности завершило логическую схему квантовой механики. Только с его помощью удалось логически непротиворечиво осуществить высший синтез дополнительных пар понятий: волна — частица, непрерывность — дискретность, причинность — случайность, явление — наблюдение. Лишь после этого удалось наконец установить, что все эти понятия образуют неделимую систему и каждое из них зависит от контекста других. А форма ответов квантовой механики на наши вопросы зависит от того, какую сторону атомного явления мы хотим изучить пристальнее.
Изучая природу, мы всегда — сознательно или бессознательно — расчленяем ее на две части: система + наблюдатель. Разделение это неоднозначно и зависит от того, какое явление мы изучаем и что мы хотим о нем узнать.
Если под явлением мы понимаем движение отдельной частицы, то это событие дискретно, случайно и большей частью ненаблюдаемо. Но если явление мы называем результат наблюдения за движением многочисленных одинаковых атомных объектов, то это событие непрерывно, закономерно и описывается волновой функцией.
Квантовая механика изучает только такие события. Для них она дает достоверные и однозначные предсказания, которые до сих пор ни разу не были опровергнуты опытом.
ВОКРУГ КВАНТА
ЛЮДИ, СОБЫТИЯ, КВАНТЫ
Результаты науки не зависят от психологии или желаний отдельных людей, и в этой объективности — ее сила и ценность. И все же наука — дело человеческое, и оттого ее история — это не только развитие физических понятий и математических методов, но также история человеческих судеб. Рядом с открытиями любая подробность жизни ученых выглядит значительной: мы всегда стремимся понять, как та или иная мелочь, из которых складывается повседневная жизнь великих людей, повлияла на дела, которые их обессмертили.
История создания квантовой механики сохранила для нас несколько живых воспоминаний, которые помогают представить ту обстановку напряжения и подъема, в которой люди разных национальностей, возрастов и темпераментов всего за три года построили современное здание квантовой механики.
Быть может, все началось с того, что в конце мая 1925 года Вернер Гейзенберг заболел сенной лихорадкой и по совету своего тогдашнего руководителя Макса Борна уехал отдыхать на остров Гельголанд в Балтийском море. Там у него было время проделать подробные вычисления, без которых не удавалось разрешить давно мучившую его идею. Уже 5 июня, по возвращении из отпуска, он написал о своих вычислениях Кронигу, а 24 июня — подробное письмо Паули, в котором содержалось начало будущей матричной механики. Правда, математическая культура Гейзенберга уступала глубине его физических идей: он не знал даже, что величины, которые он тогда ввел, в математике уже давно известны под названием матриц. Поэтому сформулировать теорию Гейзенберга математически строго удалось лишь с помощью Макса Борна и совсем молодого тогда Паскуаля Иордана. Уже в июле они завершили в Геттингене построение матричной механики.
Независимо от них в Кембридже ту же задачу решил Поль Дирак, который летом 1925 года на семинаре у Петра Леонидовича Капицы слушал доклад Гейзенберга, посетившего Англию вскоре после выздоровления.
С помощью этой новой математики осенью того же года Вольфганг Паули нашел уровни энергии атома водорода и доказал, что они совпадают с уровнями атома Бора.
В то же лето Гаудсмит и Уленбек предложили гипотезу о спине электрона, Луи де Бройль окончательно разработал идею о волнах материи, а Эльзассер и Эйнштейн посоветовали объяснить с помощью этих теорий эксперименты Дэвиссона и Кенсмена по отражению электронных пучков от поверхности металлов.
Волновая механика родилась год спустя, весной 1926 года. Ее встретили недоверчиво, поскольку в ней явно отсутствовали квантовые скачки — то, к чему лишь недавно и с большим трудом привыкли и что считалось главной особенностью атомных явлений.
В июне 1926 года Гейзенберг приехал в Мюнхен навестить родителей и «...пришел в совершенное отчаяние», услышав на одном из семинаров доклад Эрвина Шредингера и его интерпретацию квантовой механики.
Споры о волновой механике продолжались часами и днями и достигли предельной остроты в сентябре 1926 года, когда Шредингер приехал по приглашению Бора в Копенгаген.
Шредингер настолько устал от дискуссий, что даже заболел и несколько дней провел в доме Бора, который в течение всей болезни гостя почти не отходил от его постели.
Время от времени, характерным жестом подняв палец, Нильс Бор повторял:
— Но, Шредингер, вы все-таки должны согласиться... Однажды почти в отчаянии Шредингер воскликнул:
— Если мы собираемся сохранить эти проклятые квантовые скачки, то я вообще сожалею, что имел дело с атомной теорией!
— Зато остальные весьма признательны вам за это, — ответил ему Бор.
С течением времени точки зрения сторонников матричной и волновой механик сближались. Сам Шредингер доказал их математическую эквивалентность, а Макс Борн летом 1926 года догадался, какой физический смысл следует приписать ψ-функции Шредингера.
Опыты по дифракции электронов, ставшие известными осенью 1926 года, сильно укрепили веру в теории де Бройля и Шредингера. Постепенно физики поняли, что дуализм «волна-частица» — это экспериментальный факт, который следует принять без обсуждений и положить его в основу всех теоретических построений.
Теперь ученые старались понять, к каким следствиям приводит этот факт и какие ограничения он накладывает на представления об атомных процессах. При этом они сталкивались с десятками парадоксов, понять смысл которых зачастую не удавалось.
В ту осень 1926 года Гейзенберг жил в мансарде физического института в Копенгагене. По вечерам к нему наверх поднимался Бор, и начинались дискуссии, которые часто затягивались за полночь. «Иногда они заканчивались полным отчаянием из-за непонятности квантовой теории уже в квартире Бора за стаканом портвейна, — вспоминал Гейзенберг. — Однажды после одной такой дискуссии я, глубоко обеспокоенный, спустился в расположенный за институтом Фэллед-парк, чтобы прогуляться на свежем воздухе и немного успокоиться перед сном. Во время этой прогулки под усеянным звездами ночным небом у меня мелькнула мысль, не следует ли постулировать, что природа допускает существование только таких экспериментальных ситуаций, в которых... нельзя одновременно определить место и скорость частицы».
В этой мысли — зародыш будущего соотношения неопределенностей.
Быть может, чтобы снять напряжение этих дней, в конце февраля 1927 года Нильс Бор уехал в Норвегию отдохнуть и походить на лыжах. Оставшись один, Гейзенберг продолжал напряженно думать. В частности, его очень занимал давний вопрос товарища по учебе, сына известного физика Друде: «Почему нельзя наблюдать орбиту электрона в атоме при помощи лучей с очень короткой длиной волны, например гамма-лучей?»
Обсуждение этого эксперимента довольно быстро привело его к соотношению неопределенностей, и уже 23 февраля он написал об этом Паули письмо на 14 страницах.
Через несколько дней возвратился из отпуска Бор с готовой идеей дополнительности, которую он окончательно продумал в Норвегии.
Еще через несколько недель напряженных дискуссий с участием Оскара Клейна все пришли к выводу, что соотношение неопределенностей — это частный случай принципа дополнительности, для которого возможна количественная запись на языке формул.
В последующие месяцы интерпретация математического формализма квантовой механики дополнялась и уточнялась и окончательно утвердилась в Брюсселе на Сольвеевском конгрессе осенью 1927 года. На этот конгресс собрались Планк, Эйнштейн, Лоренц, Бор, де Бройль, Борн, Шредингер, а из молодых — Гейзенберг, Паули, Дирак, Крамерс. Это была самая суровая проверка всех положений квантовой механики. Она ее с честью выдержала и с тех пор почти не претерпела никаких изменений.
В те годы в Копенгагене, в институте Бора, была создана не только наука об атоме — там выросла интернациональная семья молодых физиков. Среди них были Гейзенберг, Паули, Крамерс, Гамов, Ландау, Гаудсмит и многие другие. Беспримерное в истории науки содружество ученых отличали бескомпромиссное стремление к истине, искреннее восхищение перед величием задач, которые им предстояло решить, и неистребимое чувство юмора, которое так гармонировало с общим духом интеллектуального благородства: «Есть вещи настолько серьезные, что о них можно говорить лишь шутя», — любил повторять Нильс Бор. который стал их учителем и духовным отцом.
Через много лет политические бури разбросают их по всему миру: Гейзенберг станет главой немецкого «уранового проекта»; Нильс Бор, спасаясь от нацистов, окажется в американском центре атомных исследований в Лос-Аламосе, а Гаудсмита назначат руководителем миссии «Алсос», которая будет призвана выяснить, что успел сделать Гейзенберг для постройки немецкой атомной бомбы.
Сейчас этих людей осталось совсем немного, и вместе с ними из жизни уходит целая эпоха в физике, которую можно сравнить лишь с эпохами Галилея и Ньютона.
|
ПОИСК:
|