
Кинетическая теория газов
Пытаться описывать движение каждого атома в отдельности - дело безнадежное, да и не нужное: никакой прибор не может уследить за всеми атомами. Еще в середине XIX века поняли, что к системам, состоящим из очень большого числа частиц, надо подходить с точки зрения теории вероятностей, рассматривая не свойства отдельных атомов, а усредняя эти свойства по большой их совокупности.
Во второй половине XIX века возникла новая наука - статистическая физика, достигшая своего расцвета в работах Больцмана и Гиббса.
Однако первые идеи зародились раньше. В этой связи стоит рассказать о замечательной истории англичанина Уотерстона.
В 1845 г. в английскую академию наук (ее называют Лондонским Королевским обществом) была представлена работа Уотерстона. В ней было показано, что давление газа на стенки сосуда можно объяснить ударами атомов.
Хотя сама идея о том, что газ состоит из атомов, была не нова, мало кто принимал всерьез утверждения, что атомы могут свободно двигаться в сосуде от стенки к стенке, а упругие свойства газа можно свести просто к классической механике атомов. Работа Уотерстона не понравилась членам ученого общества и была ими отклонена. Лишь много лет спустя ее нашел в архиве Релей* и опубликовал в 1892 г. в журнале Королевского общества, который выходит и в наши дни.
* (Релей - английский физик, один из создателей теории колебаний и, в частности, теории звука.)
Релей, между прочим, заметил, что Уотерстон поступил не предусмотрительно, не рассказав в начале статьи о своих предшественниках. Между тем, еще Д. Бернулли в 1727 г. писал о связи давления газа с квадратом скорости движения его частиц. Если бы Уотерстон упомянул своего великого предшественника, то, как писал Релей, у рецензента Королевского общества не хватило бы смелости объявить работу "бессмысленной, непригодной даже для чтения перед обществом".
Это был печальный эпизод. То, что было сделано одним человеком и осталось незамеченным, было открыто впоследствии лишь в результате деятельности нескольких людей, а окончательная формула была написана Максвеллом только в 1859 г.
История эта поучительна. Сколько труда было потрачено на то, чтобы получить очень простую, на наш взгляд, формулу;
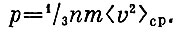
Здесь р - давление газа, п - количество молекул в 1 см3 (концентрация газа), т - масса молекулы, 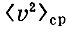 - среднее арифметическое квадратов скоростей молекул.
- среднее арифметическое квадратов скоростей молекул.
|
ПОИСК:
|