
Максимальная температура
Появление отрицательных температур - не единственный сюрприз, преподнесенный квантовой механикой.
Мы знаем, что не всегда нагревание тела сопровождается повышением его температуры. Когда тает лед, то поступающая теплота уходит на превращение льда в воду, на разрушение кристаллов. Удельная теплота плавления льда -81 ккал/кг-3,4*103 Дж/кг - это энергия, которая уходит на разрушение связей в кристалле. Только после того, как лед весь расплавится, температура начнет повышаться и будет повышаться до тех пор, пока приток тепла не прекратится. Такой же процесс можно наблюдать при 100 °С, когда вода начнет кипеть. Фазовые переходы лед→вода, вода→пар иллюстрируют различие между теплотой и температурой. Только для одноатомного газа энергия системы пропорциональна температуре: ?mv2=3/2кТ, в более сложных системах энергия и температура - разные характеристики теплового состояния тела.
На примере атомного ядра мы видели, что температура связана с плотностью состояний энергии в системе.
Эта связь описывается формулой
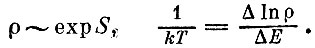
Как зависит плотность уровней р (или ее логарифм lnp) от энергии, в общем виде сказать нельзя - у каждой физической системы свое распределение уровней.
Не задумываясь пока о физическом смысле формул, предположим, что р зависит от энергии по закону lnр ∼ΔЕ или р∼ехр(ΔЕ), где А - какая-то постоянная величина. Система с таким свойством обладает удивительной особенностью - ее температура не зависит от энергии. Действительно, для принятой зависимости lnр от Е изменение lnp пропорционально изменению Е и температура определится формулой
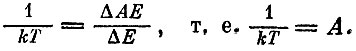
Система будет поглощать тепло без какого-либо повышения температуры: можно сказать, что она характеризуется бесконечной "скрытой теплотой". Отсюда следует, что если у какой-либо системы логарифм плотности состояний при большой энергии стал пропорциональным самой энергии, температура такой системы стремится к постоянному значению. У такой системы существует максимальная температура, выше которой ее нельзя нагреть, сколько бы мы ни подводили к ней тепла. Этот пример помогает понять смысл температуры. Количество теплоты, поглощенной телом, расходуется двумя разными путями. В классической физике времен Максвелла и Больцмана считалось, что энергия распределяется между степенями свободы частиц так, что каждая поступательная (и вращательная) степень свободы получает по 1/2kT энергии, а каждое из колебаний - кТ (из которых 1/2кТ уходит в потенциальную энергию). Число степеней свободы, т. е. число координат, которым определяется положение молекулы в пространстве, естественно, задано. Поэтому, вступая в противоречие с опытом, классическая статистика приходила к выводу, что теплоемкость не зависит от температуры и что на повышение температуры на один градус, скажем, газа, требуется затратить одно и то же количество теплоты.
В квантовой механике выяснилось, что в процессе создания теплового равновесия участвуют не все степени свободы; напротив, существуют "замороженные" степени свободы, которые вступают в игру только с повышением температуры.
Таким образом, часть тепла уходит не на увеличение кинетической и потенциальной энергии, а на создание новых степеней свободы. Во время фазового перехода лед - вода на это уходит вся подводимая теплота. Поэтому температура остается постоянной. В одноатомном газе, напротив, вся теплота уходит на кинетическую энергию атомов.
Надо подчеркнуть, что описанная система с максимальной температурой не может быть реализована потому, что процесс создания новых степеней свободы не может продолжаться бесконечно долго, - система в конце концов испарится.
|
ПОИСК:
|