
§ 15. Измерение скорости молекулы газа
Используя основное уравнение кинетической теории газа, вычислим среднюю квадратичную скорость движения молекулы газа.
В формуле 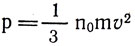 произведение числа молекул в единице объема на массу молекулы есть плотность газа ρ, поэтому
произведение числа молекул в единице объема на массу молекулы есть плотность газа ρ, поэтому 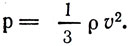 Отсюда
Отсюда
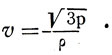
При нормальных условиях р = 1 атм = 1,01*105н/м2, плотность водорода р = 0,00009 кг/мг. Средняя квадратичная скорость движения молекул водорода
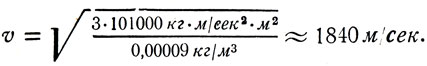
Так можно вычислить скорость молекул различных газов.
Опытным путем скорость движения молекул газа впервые определил в 1920 г. немецкий физик Штерн. При вращении столика струя воды падает позади стаканчика (рис. 15, а). Подобное явление использовал Штерн. Жестко скрепленные внешний цилиндр 1 и внутренний 2 электродвигателем могут быть приведены во вращение вокруг общей оси 001 (рис. 15, б). По оси протянута проволока 3, покрытая серебром. Параллельно проволоке во внутреннем цилиндре прорезана узкая щель 4. Прибор помещался под воздушный колокол, из которого откачивался воздух, чтобы молекулы серебра меньше сталкивались с молекулами газов. Цилиндры неподвижны. Проволоку нагревают током. Серебро начинает испаряться. Из цилиндра 2 выходят только те молекулы (атомы) серебра, которые попадают в щель, они на цилиндре 1 дают узкую полоску 5 налета серебра.
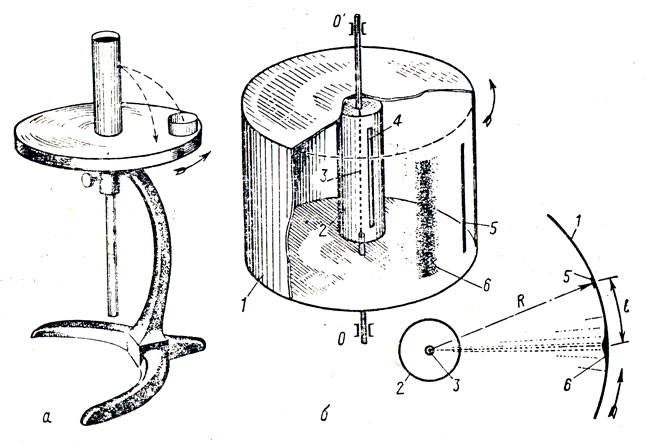
Рис. 15. Схема опыта Штерна
При вращении цилиндров налет серебра 6 получается размытым и смещенным на l (берется середина полоски) от полоски 5 в сторону, противоположную направлению вращения цилиндра. Размытость полосы говорит о том, что молекулы серебра имели различные скорости: более быстрые раньше достигали цилиндра 2 и оседали ближе к полоске 5, более медленные - дальше от нее.
Время, за которое молекула пролетает от проволоки до стенки цилиндра
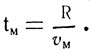
Время, за которое цилиндр смещается на l, равно смещению, деленному на линейную скорость вращения точек цилиндра:
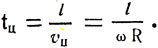
Время прохождения молекулой пути R и время поворота цилиндра на l равны между собою, поэтому
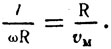
Отсюда скорость молекулы
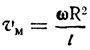
или
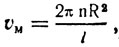
где n - число оборотов цилиндра за 1 сек.
По теоретическим расчетам средняя квадратичная скорость молекул паров серебра при t° = 1200° С равна 580 м/сек. В опыте Штерна она оказалась 576 м/сек. Такое совпадение теоретического значения скорости со значением, полученным из опыта, подтверждает правильность молекулярно-кинетической теории газов.
|
ПОИСК:
|