
Атом в Манчестере
Профессор физики Манчестерского университета Артур Шустер, перед тем как выйти в отставку, предложил на освобождаемую им должность пригласить Резерфорда. Совет университета единогласно избрал Резерфорда профессором кафедры физики и послал ему в Монреаль официальное приглашение, которое, конечно, было принято.
В мае 1907 г. Резерфорд с женой и шестилетней дочерью Эйлин-Мери выехали в канадский порт Квебек, откуда на пароходе "Императрица Ирландии" они отплыли в Англию.
Манчестерский университет получил статус самостоятельного высшего учебного заведения в 1903 г. Раньше это было отделение университета Королевы Виктории, в состав которого, кроме Манчестерского, входили отделения в Ливерпуле и Лидсе. Кафедрой физики в XIX веке руководили Джон Дальтон и Джемс Прескот Джауль. Физическая лаборатория, заведовать которой должен был Резерфорд, была основана в 1900 г. Вскоре после приезда Резерфорд писал в письме к матери, что лаборатория очень хороша, хотя и не строилась на такие щедрые средства, как монреальская. До приезда Резерфорда в этой лаборатории велись главным образом низкотемпературные (криогенные) исследования, например, изучались физические свойства жидкого воздуха и различных газов.
В лаборатории Резерфорд прежде всего познакомился с молодым научным сотрудником, приехавшим недавно из Германии, Гансом Гейгером и новозеландцем Робинсоном, а также студентом-физиком Томасом Ройдсом, специализировавшимся по спектроскопии под руководством Шусте-ра и позднее принявшим участие в экспериментах по идентификации альфа-частиц с атомами гелия.
Резерфорд сразу приступил к работе в лабораторий, начав с подготовки оборудования установок для своих опытов. Робинсон говорил, что Резерфорд был очень требователен к аппаратуре. Он оборудовал установку для изучения эманации менее чем за три недели после того, как покинул Монреаль.
Гейгер занимал должность научного сотрудника по физике. Он почти не принимал участия в обучении студентов; его обязанностью была исследовательская работа. Резерфорд предложил ему заняться осуществлением идеи ионизационного метода счета альфа-частиц и впоследствии созданные Гейгером ионизационные счетчики частиц навсегда вписали его имя в историю физики XX века.
Одновременно Гейгер помогал Резерфорду проводить опыты по счету сцинтилляций, возникающих при падении альфа-частиц на люминесцирующий экран.
Эти опыты были начаты в 1908 г. после того, как Венская академия наук прислала для нужд манчестерской лаборатории 400 миллиграммов радия (за которые через двадцать лет Кембриджский университет уплатил 3000 фунтов). Не так просто было хранить и подготовить к опытам этот драгоценный запас радия, и поэтому Резерфорд убедил своего друга профессора Б. Болтвуда приехать на время из Монреаля в Манчестер и помочь ему. Вдвоем они создали аппаратуру для обезвоживания радиоактивных солей и очистки радона от примесей. Были также приняты меры для хранения радия в течение длительного срока с достаточной безопасностью для персонала лаборатории.
В 1909 г. Резерфорд при участии Гейгера и Ройдса произвел серию опытов, которые еще с большей очевидностью подтвердили его убеждение, что альфа-частицы есть не что иное, как дважды ионизованные (т. е. потерявшие по два электрона) атомы гелия. Напомним, что к этому убеждению Резерфорд пришел еще в Монреале, когда он с помощью электроскопа и системы металлических пластинок с малыми зазорами показал, что масса альфа-частиц больше массы водорода, и довольно точно измерил отношение их заряда к массе. Из этого отношения можно было сделать вывод, что альфа-частицы - это, по-видимому, ионизованные атомы гелия.
Однако несмотря на то, что такое определение идентичности альфа-частиц и атомов гелия было вполне достоверным, Никто не видел еще гелия, родившегося из радия, и поэтому многие ученые продолжали относиться с сомнением к утверждению Резерфорда, хотя оно и было экспериментально подтверждено. Стремление еще более наглядно показать такую идентичность, привело Резерфорда к идее другого опыта. Практическое выполнение его несложно, но именно это еще раз подтверждает не только удивительное экспериментальное искусство великого ученого, но и необыкновенную глубину его мышления.
В наше время в физике ядра м элементарных частиц широко пользуются косвенными экспериментами, тем не менее дающими бесспорные представления о том или ином явлении (доказательность таких опытов в значительной мере определяется высоко развитой экспериментальной техникой, какая не существовала во времена Резерфорда).
Но тогда Резерфорд считал своим долгом физика, этому способствовал его склад ума, продемонстрировать гелий, образующийся при альфа-распаде радиоактивных веществ, так же наглядно, как это делают в университетских лабораториях с существенными количествами этого аза, например, с помощью методов спектроскопии. Такой "высшей" степени наглядности вполне соответствовали опыты, осуществленные им в манчестерской лаборатории.
В запаянной стеклянной трубке 2 находится некоторое количество радона. Стенки трубки имеют толщину всего 0,01 миллиметра. Они достаточно тонки, чтобы испускаемые радоном альфа-частицы могли проходить через них во внешнюю трубку 3. Перед опытом трубка 3 тщательно откачивалась, и в ней спектрографическим путем нельзя было обнаружить линий гелия.
Через несколько дней исследователи могли обнаружить во внешней трубке 3 накопление какого-то газа. Повышая давление в приборе, этот газ концентрировали в разрядной трубке 1. Через эту трубку пропускался электрический разряд. Спектральным анализом в ней можно было установить полный спектр гелия, т. е. в разрядной трубке был гелий.
Но может быть гелий попал в трубку 2 по недосмотру вместе с радоном, а оттуда проник в трубки 3 и 1? Контрольный опыт дал на этот вопрос отрицательный ответ. Используя точно такой же прибор для контрольного опыта, Резерфорд помещал в трубку 2 не радон, а чистый гелий. Однако через несколько дней в разрядной трубке спектральных линий гелия не обнаруживалось. Гелий не мог пройти через стеклянные стенки трубки 2 в трубку 3.
Альфа-частицы же легко проходили через тонкое стекло и накапливались в трубках 3 и 1, давая при разряде характерные линии гелия.
Этот опыт Резерфорда, в котором точно идентифицировались альфа-частицы с атомами гелия, уже ни у кого не мог оставить и тени сомнения в правильности теории радиоактивного распада, выдвинутой Резерфордом и Содди в Мак-Гиллском университете и, в частности, в том, что атомы некоторых химических элементов, расположенных в конце периодической системы, самопроизвольно распадаются, и в этом процессе происходит превращение одних элементов в другие.
После этих опытов внимание многих физиков было привлечено к гелию, который был впервые открыт на Солнце. Сначала астрономы и астрофизики открыли этот инертный газ по его желтым спектральным линиям, оказавшимся в спектре солнечных лучей. Затем В. Рамсей выделил гелий из минералов, а Резерфорд доказал, что гелий является продуктом, образующимся при альфа-распаде радия, тория, урана. Еще позже ученые выдвинули идею о том, что гелий образуется на Солнце в результате слияния более легких ядер водорода, и этот процесс, названный впоследствии термоядерной реакцией, служит источником гигантской солнечной энергии.
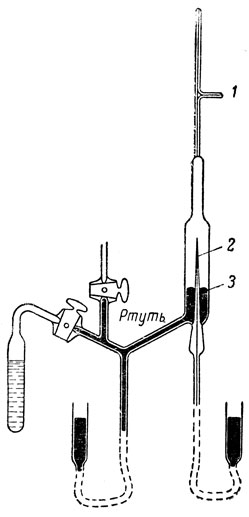
Установка для проведения опыта, доказывающего, что альфа-частицы - это атомы гелия
Исследования Резерфорда в последние годы жизни, касавшиеся взаимодействия дейтронов (ядер дейтерия), а также открытия Резерфордом совместно с Марком Олифантом и Гартеком трития (Н3) и изотопа гелия (Не3) впоследствии натолкнули ученых на мысль о возможности использования управляемых термоядерных реакций.
Если бы удалось осуществить такой синтез в лаборатории, а затем и в промышленных условиях, то человечество получило бы неиссякаемые источники дешевой энергии. Пока ядерный синтез гелия из водорода удалось осуществить только в виде мгновенного разрушительного процесса - взрыва водородной бомбы. Можно ли ориентировочно определить сроки успешного завершения опытов по использованию термоядерных реакций в мирных целях? Осенью 1963 г. академик Л. А. Арцимович, сообщая о последних успехах советских ученых в этой области, заключил свой рассказ следующими словами: "Пока еще сделан только первый шаг на пути к термоядерному синтезу, и никто не может сказать точно, удастся ли решить эту проблему за 10-15 лет. Может быть, понадобится несколько десятилетий".
Термин "термоядерные реакции" возник в пятидесятых годах, но он так же связан с возникновением атомов гелия (правда, в результате ядерного синтеза), как и понятие о радиоактивном распаде, который Резерфорд начал изучать в первые годы века и как бы символически завершил в 1908 г., когда ему была присуждена Нобелевская премия. Ученому пришлось ненадолго отвлечься от своей работы и выехать в Стокгольм.
Незадолго до этого Резерфорду исполнилось 37 лет, ему могли бы позавидовать многие лауреаты, получившие эту высокую международную научную награду в гораздо более старшем возрасте. Многие годы утомительной работы в лаборатории с радиоактивными веществами, к счастью, не повлияли на его могучее здоровье. По внешнему виду Резерфорд скорее был похож на спортсмена или агронома, постоянно проводящего время на воздухе, чем на физика-исследователя. Щеки его покрывал румянец, на лице не было ни одной морщинки, он всегда был веселым, громко хохотал, живо откликаясь на остроты.
Многим было трудно представить себе, что это один из самых выдающихся физиков мира. Незадолго до получения Нобелевской премии с ним произошел курьезный случай, виной которого была его внешность. К Резерфорду в манчестерскую лабораторию пришел Шустер с японцем и познакомил его с ученым. Японец был министром просвещения и довольно известным физиком бароном Кикучи. Позднее, оставшись наедине с Шустером, Кикучи сказал: "Я полагаю, что Резерфорд, которого вы мне представили, сын знаменитого профессора Резерфорда?". Шустер с трудом объяснил японскому физику, что этот молодой человек и есть профессор Резерфорд.
Резерфорд с женой выехал в Швецию пароходом. По дороге они ненадолго остановились в Копенгагене, где еще незнакомый Резерфорду двадцатитрехлетний физик Нильс Бор, недавно окончивший Копенгагенский университет, уже был награжден золотой медалью Датского Королевского общества за свою первую научную работу.
В Стокгольме можно было уже заметить подготовку к церемониалу вручения Нобелевских премий. Впоследствии Нобелевский лауреат, друг Нильса Бора физик-теоретик академик И. Е. Тамм говорил, что Швеция относится к этим празднествам как к событию общегосударственного значения. Вручение премий производится в торжественной обстановке по ранее выработанному и строго соблюдаемому ритуалу. Но эта торжественность не лишает простоты общения людей.
Торжество, в котором участвовал Игорь Евгеньевич Тамм при получении Нобелевской премии в 1958 г., вероятно, мало отличалось от торжественной церемонии, участником которой пятьдесят лет назад был Резерфорд.
Утром 10 декабря 1908 г. Резерфорд, одетый во фрак, вместе с женой пешком отправился из гостиницы в Концерт-хауз, где происходит вручение премий. По традиции в этот день Концерт-хауз украшен желтыми хризантемами, лавровыми венками, флагами разных стран.
Пока заполнялся зал, Резерфорд вместе с другими лауреатами стоял за кулисами. Входит королевское семейство. Все присутствующие встают. Оркестр исполняет "Песню короля". Трубачи поднимают свои инструменты - отблески от начищенной меди пробегают через зал вплоть до второго яруса, переполненного студентами.
В этот момент появляется процессия лауреатов - главных действующих лиц этого торжественного церемониала. Их сопровождают шведские академики. Лауреаты делают поклон в сторону королевской семьи и садятся в массивные кресла с высокими спинками. Это единственный случай, когда все участники церемониала, не исключая и королевской семьи, стоят, а лауреаты сидят. Министр Швеции произносит короткую речь об основателе премии - Альфреде Нобеле. Он замечает, что, несмотря на свои огромные богатства, Нобель был одиноким человеком, говорившим на многих языках, ни один из которых не был для него родным языком. Затем представитель Национальной академии наук Швеции рассказывает присутствующим о нобелевских лауреатах, о важности и достоинствах выполненных ими работ.
После этого лауреаты спускаются по ступенькам с эстрады, и король вручает каждому диплом и золотую медаль. После каждого вручения оркестр играет какое-нибудь известное классическое музыкальное произведение. В заключение церемониала исполняется шведский национальный гимн. Королевские особы выходят из зала. За ними идут лауреаты.
Вечером в "Золотом зале" городской ратуши был устроен банкет в честь лауреатов. В нем приняли участие 800 человек и вся королевская семья.
В своем тосте Резерфорд шутливо замечает: "Я имел дело со многими разнообразными превращениями с разными периодами, но самым быстрым из всех оказалось мое собственное превращение в один момент из физика в химика". Это был намек на то, что Нобелевский комитет присудил Резерфорду Нобелевскую премию по химии. Ученые все еще проявляли неуверенность, они не знали, к какой науке причислить радиоактивность: к химии или физике. Ведь кроме физиков ею продолжали активно заниматься знаменитые химики: Мари Кюри, Содди, Болтвуд, Ган и другие.
Как лауреат премии по химии Резерфорд счел нужным назвать Нобелевскую лекцию, прочитанную им в Стокгольмском университете, так: "О химической природе альфа-частиц радиоактивных веществ". Этот доклад вскоре был напечатан в "Физическом журнале" в Англии; он содержал основы новой науки, созданной Резерфордом в результате исследования альфа-радиоактивности и позднее, после открытия ядерной модели атома, получившей огромное распространение во многих странах мира под названием ядерной физики.
Проездом из Стокгольма в Манчестер Резерфорд посетил старинный голландский город Лейден, который вошел в историю мировой культуры как родина выдающихся произведений искусства и науки. Здесь работал гениальный Рембрандт, создавший величайшие шедевры живописи и основавший бессмертную голландскую школу живописи. Современная физика также во многом обязана Лейдену. В этом небольшом городе была построена лейденская банка - первый в мире конденсатор электрической энергии и разработаны знаменитые "преобразования" Лоренца, использованные Эйнштейном при создании теории относительности. В 1928 г., когда Лоренц умер, Эйнштейн произнес над его могилой речь, закончив ее словами: "Жизнь Лоренца - драгоценное произведение искусства".
Век искусства - век Рембрандта сменился величественным и трудным веком науки - веком Лоренца и Кам-мерлинг-Оннеса, сумевшего превратить в жидкость гелий. Эта смена эпох проходила и здесь, в Лейдене.
Вместе с профессором Лоренцом, которого в то время называли "отцом теоретической физики", Резерфорд осмотрел две главные достопримечательности Лейдена того времени: дом, где родился Рембрандт, и знаменитую лабораторию низких температур профессора Гейке Каммерлинг-Оннеса, в которой была установлена первая в мире машина для превращения в жидкость самого неподатливого в этом отношении газа - гелия.
В письме к Отто Гану от 22 декабря 1908 г. Резерфорд писал: "Мы приехали в Амстердам в субботу около 8.30 утра и в 12.30 выехали в Лейден, где пробыли до 9 часов вечера вместе с профессором Лоренцом, осматривая старый город и лаборатории. Я видел машину Каммерлинг-Оннеса для производства жидкого гелия, но не было времени повидаться с людьми. Затем мы совершили большое путешествие в Харвич и прибыли домой в 4.30 в воскресение после длинного и медленного путешествия в субботних поездах по Англии".
Резерфорд проявлял большой интерес к работам Каммерлинг-Оннеса и особенно к его методам получения жидкого гелия. Видимо, после своих опытов по получению жидкого радона, успешно проведенных в Монреале, он предполагал, что низкотемпературные исследования приобретут важную роль в изучении вопросов строения вещества. И он не ошибся.
Много лет спустя Резерфорд, будучи уже директором Кавендишской лаборатории, принял деятельное участие в организации специальной лаборатории имени Монда при Королевском обществе в Кембриджском университете, директором которой стал П. Л. Капица. Он совмещал эту должность с обязанностями помощника директора Кавендишской лаборатории с 1924 по 1932 год. Мондская лаборатория была предназначена для проведения широких исследований в области низких температур и имела уникальное для тех лет оборудование.
В настоящее время низкие температуры, получаемые с помощью жидкого гелия и жидкого водорода, совершенно необходимы в экспериментах по ядерной физике (как, впрочем, и во многих других областях, например в кибернетике). Многие явления, связанные с взаимодействием элементарных частиц, нельзя было бы обнаружить, не применяя низких температур.
Вернувшись из Швеции, Резерфорд вместе с Гейгером приступил к новым экспериментам, результаты которых произвели новый и, пожалуй, один из самых значительных научных переворотов в физике первой половины XX столетия.
Изучение радиоактивного альфа-распада к этому времени было в основном завершено, оставались вопросы, которые можно было решить, только перейдя на новые ступени физики. К ним и вели опыты, начатые Резерфордом после получения Нобелевской премии. Присуждение этой премии Резерфорду через несколько лет после того, как ее получили Беккерель и супруги Кюри, указывало на то, что научная общественность всего мира высоко оценила важность изучения радиоактивного процесса и поняла далеко идущие перспективы, связанные с ним. Теперь уже очень многие физики и химики в различных странах займутся исследованиями в этой области.
Резерфорд и Гейгер продолжали опыты по наблюдению сцинтилляций, вызываемых альфа-частицами, падающими на люминесцентный экран. Еще в первом издании своей книги "Радиоактивные вещества и их излучения" Резерфорд писал, что наблюдение сцинтилляций на экране из сернистого цинка представляет собой очень удобный способ счета частиц, если каждая частица вызывает вспышку.
Опыты, продолжавшиеся в манчестерской лаборатории, привели Резерфорда к заключению, что каждая сцинтилляция (вспышка) вызывается одной альфа-частицей.
Так, впервые физики получили возможность наблюдать за поведением отдельных атомов. Эти опыты поражали воображение, они создали Резерфорду особую популярность в научном мире.
Резерфорд и Гейгер подсчитали методом визуального счета сцинтилляций, что в одну секунду из излучателя весом в одну тысячную грамма радия вылетает 130 тысяч альфа-частиц. Этот подсчет, точность которого была безукоризненной, лишний раз убеждал Резерфорда в том, что поток альфа-частиц может служить прекрасным средством проникновения в атом. И действительно, в последующие годы альфа-частицы были важнейшим орудием ученого в исследованиях, результатами которых было открытие ядерного строения атома и ядерных реакций.
По многу часов Резерфорд и Гейгер, а затем и Марсден проводили в затемненной лаборатории за утомительным счетом сцинтилляций. Гейгер рассказывал, что ему одному пришлось посчитать в общей сложности миллион альфа-частиц.
В статье о Резерфорде Гейгер писал: "Я вспоминаю его таинственную лабораторию в верхней части здания, под самой крышей. В ней хранился запас эманации и здесь им были выполнены многие известные работы по ее изучению. В памяти возникает также мрачный погреб, в котором Резерфорд устанавливал свои чувствительные приборы для изучения альфа-частиц. Тот, кто спускался туда по двум ступенькам, прежде всего слышал в темноте голос профессора, предупреждавшего, что помещение пересекает на высоте головы горячий трубрпровод, и, кроме того, необходимо осторожно, чтобы не упасть, перешагнуть две водопроводные трубы. После этого, наконец, в слабом свете вошедший различал самого Резерфорда, сидящего у приборов. Тотчас же великий ученый мог начать рассказывать в собственном неподражаемом стиле о развитии своих опытов и о трудностях, которые приходится преодолевать...".
Однажды Резерфорд поручил Марсдену считать альфа-частицы, проходящие через тонкие металлические пластинки, которые помещались в прибор (его называли спинтарископом) между излучателем частиц и экраном.
Резерфорд сказал молодому человеку, что вряд ли он обнаружит что-либо любопытное. Можно было предвидеть, что альфа-частицы будут легко проходить через пластинки, если, конечно, правильна модель атома Томсона. Но пока не было оснований сомневаться в этом. Марсден приступил к опытам, используя для них коническую трубку 1 с радоном, установленную под углом к тонкой металлической пластинке 2.
Свинцовый блок 5 преграждал путь альфа-частицам, испускаемым радоновым излучателем, к сцинтилляционному экрану 3. Микроскоп 4 служил для наблюдения возможных сцинтилляций, которые могли возникнуть при отклонении альфа-час-гиц от металлической пластинки.
И, действительно, Марсден обнаружил, что некоторые альфа-частицы, а таких было незначительное количество, отскакивали от пластинки назад в направлении излучателя. Такое поведение альфа-частиц удивило Марсдена, и он продолжал опыты, чтобы убедиться в том, что диффузное рассеяние не представляло собой поверхностного эффекта и что альфа-частицы проникали внутрь металлической пластинки и лишь затем немногие из них отклонялись на угол в 150°, т. е. почти возвращались к излучателю. Это подтверждалось тем, что количество отклоняющихся на большие углы частиц увеличивалось с увеличением толщины пластинки.
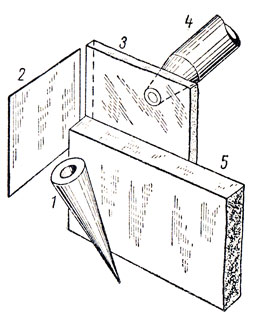
Опыт Резерфорда и Марсдена по рассеянию альфа-частиц
Марсден рассказал Резерфорду об этих результатах, не согласующихся с обычными представлениями о структуре атома, предложенными Томсоном. Впоследствии Резерфорд признался, что наблюдавшиеся Марсденом единичные альфа-частицы, которые отскакивали от металлической пластинки, произвели на него потрясающее впечатление.
"Это было почти неправдоподобно,- говорил Резерфорд,- как если бы вы выстрелили пятнадцатифунтовым снарядом в кусок папиросной бумаги и снаряд отскочил бы обратно и поразил вас".
Результаты опытов Марсдена прежде всего натолкнули Резерфорда на мысль, что модель атома Томсона, принятая всеми учеными в качестве наиболее достоверной, на самом деле может быть подвергнута серьезным сомнениям.
Действительно, модель Томсона, согласно которой положительный заряд распределен по всему объему атома и уравновешивается отрицательным зарядом электронов с массой гораздо меньше массы альфа-частиц, не позволяла представить себе происходящего даже и в редких случаях отклонения альфа-частиц, бомбардирующих металлическую пластинку. В этом случае естественно было бы ожидать, что альфа-частица, столкнувшись с гораздо более легким, чем она сама, электроном, может лишь незначительно отклониться от своего прямолинейного пути, но не способна получить мощный толчок, выбрасывающий ее за пределы атома мишени под большим углом к начальному направлению, достигающим 150°, т. е. почти в обратную сторону.
Мощный толчок, отбрасывающий альфа-частицу, мог быть получен только в том случае, если она натолкнулась бы на какую-то массивную преграду, имеющуюся в атоме. Огромное же большинство альфа-частиц, видимо, не встречая такого препятствия, легко проходило через свободное пространство, имеющееся в атоме.
Так у Резерфорда возникли идеи о другой структуре атома, совершенно отличающейся от той, которая мыслилась Томсоном. Через три недели после беседы с Марсденом Резерфорд уже теоретически рассчитал, что рассеяния альфа-частиц, наблюдавшиеся его учеником, могут быть объяснены существованием в атоме массивной части, которую он назвал ядром (nucleuc), возможно, использовав термин, принятый в биологии и обозначающий центральную часть живой клетки (ядро клетки).
В предложенной Резерфордом модели атома ядро, представляющее собой маленькую массивную часть, расположено в центре системы, а вокруг него по орбитам вращаются легкие электроны.
Согласно модели атома Резерфорда атом представляет собой как бы миниатюрное подобие солнечной системы, в которой положительно заряженное ядро играет роль центрального светила, т. е. солнца, а электроны, несущие отрицательный заряд, - миниатюрные планеты, вращающиеся вокруг ядра под действием электрических сил кулоновского притяжения. Поэтому вначале она была названа планетарной моделью. Ее также называли нуклеарной, т. е. ядерной, моделью.
После открытия Резерфордом ядра в течение нескольких десятилетий модель атома Томсона оставалась лишь достоянием истории физики XX века. Но здесь, прерывая ход повествования о развитии ядерной физики, хочется упомянуть о достижениях физики пятидесятых и шестидесятых годов, когда случилось нечто поразительное, заставившее ученых вновь обратиться к модели Томсона.
В последние годы, когда в результате интенсивных исследований с помощью мощных ускорителей и других эффективных средств необычайно расширились сведения об элементарных частицах, их взаимодействиях и выяснились некоторые важные закономерности, физики обнаружили атомы, строение которых согласуется с моделью Томсона. Это довольно хорошо уже изученные мезоатомы, составляющие одну из наиболее удивительных форм вещества.
Было установлено, что частицы - мезоны с отрицательным зарядом, открытые Юкавой, могут входить в состав атомов, выполняя роль отрицательно заряженных электронов в обычных системах. Мезоны притягиваются положительным зарядом ядра, чем создается стабильность мезоатома.
Так же как электрон, мезон может находиться в различных состояниях движения вокруг ядра, и при переходе из одного состояния в другое, более прочно связанное, происходит испускание фотона - кванта света. Такой мезоатом может образовать и частица пи-мезон и частица мю-мезон. Движение мю-мезона, например, в мезоатоме очень похоже на движение электрона. Силы, действующие на мю-мезон, это в основном те же электрические силы, которые действуют и на электрон.
Масса мю-мезона примерно в 200 раз больше массы электрона. Известно, что радиус орбиты ближайших к ядру электронов (строго говоря, среднее расстояние электрона от ядра) должен быть обратно пропорционален массе электрона. Отсюда следует, что радиус орбиты мю-мезона в 200 раз меньше, чем электрона.
Рассматривая атомы тяжелых элементов, у которых заряд ядра очень большой, видим, что у них радиус орбиты ближайших к ядру электронов очень мал. Если представить себе вместо электрона мю-мезон, то этот очень малый радиус нужно уменьшить еще в 200 раз и тогда окажется, что он меньше радиуса ядра. Можно было бы думать, что в этом случае мезоатом невозможен, так как ядро, в котором сосредоточена почти вся масса атома, трудно проницаемо для частиц. Но мезоатомы тяжелых элементов существуют - это бесспорно доказано. В них мезон действительно движется внутри ядра и, как ни странно, движется свободно.
Таким образом, физики показали, что возможен атом, совсем не похожий на планетарную модель, которая после знаменитых опытов Резерфорда и разработки квантовых представлений Бором стала не только привычной, но и на определенном этапе развития науки казалась единственно возможной. Отрицательно заряженная частица (пока это относится к мезону), движущаяся в самом ядре, воз-* вращает нас к модели атома Томсона.
Такое отступление в последовательном рассказе о строении ядра, представления о котором развивались вместе с исследованиями Резерфорда и, можно сказать, много лет зависели от них, понадобилось по нескольким причинам.
Прежде всего, читатель, знакомясь с историей жизни и научных достижений Резерфорда, не должен забывать о любых самых поразительных изменениях, возникающих время от времени в процессе прогресса науки и заставляющих коренным образом менять представления о физических явлениях, их сущности и механизме.
Нужно помнить и о том, что часто открытия, сделанные подлинно талантливыми учеными, могут быть забыты и довольно надолго, но может также наступить день, когда именно они дадут толчок новым выдающимся исследованиям или будут использованы для создания новых областей науки и техники. Примером этого могут служить и ранние работы Резерфорда по изучению легких ядер, о которых говорил Курчатов в Англии.
Второе рождение модели Томсона - предшественницы модели Резерфорда приводит, естественно, к мысли о том, как глубоки и проницательны были опыты и теоретические построения этого выдающегося учителя Резерфорда - "кавендишского профессора" Джозефа Томсона в области строения вещества. Несомненно и то, что острота и сила научного мышления Томсона сыграла большую роль в формировании исследовательского таланта Резерфорда и возбудила в молодом новозеландце интерес к самым сложным явлениям природы, какими в то время считались, да и сейчас считаются, проблемы строения вещества и процессов, происходящих в атомах и атомных ядрах.
Примеру Резерфорда, применившего для атома термин "ядро", принятый в биологии, спустя много лет последовал ученик и сотрудник Нильса Бора Отто Фриш, который перенес в ядерную физику из биологии другой термин - "деление", обозначающий там процесс размножения клетки. Фриш назвал делением процесс разрушения на два примерно равных осколка ядер урана, тория, плутония. Теперь все эти вещества, применяемые как ядерное горючее в ядерных реакторах, получили название делящихся материалов.
Сейчас, в век ядерной энергии, пожалуй, не стоит подробно объяснять, какое величайшее значение для науки имело открытие Резерфордом атомного ядра, но и в то время оно было высоко оценено и тотчас же вызвало во многих странах интерес и энтузиазм у многих крупных физиков, которые увидели в новом открытии широкие перспективы для познания строения вещества.
Сотрудник Резерфорда известный английский физик-теоретик Чарлз Дарвин писал: "Я считаю одним из величайших событий своей жизни то, что произошло в моем присутствии спустя полчаса после "рождения" ядра. Это было во время воскресного ужина в манчестерской квартире Резерфорда. Я помню, как он говорил нам, что наблюдаемое большое рассеяние альфа-частиц показывает на существование в атоме необычайно могучих сил".
Представления об атоме, выдвинутые Резерфордом в виде планетарной модели и быстро получившие дальнейшее развитие, заключались в следующем. Атом в нормальном (неионизованном) состоянии нейтрален, так как в целом он содержит столько же положительного электричества (заряд ядра), сколько и отрицательного (заряд электронов). Он имеет Z электронов, каждый с зарядом е, и, следовательно, ядро должно иметь заряд +Z е. Атом одного элемента должен отличаться от атома другого элемента количеством электронов или, что то же самое, целым числом Z единичных зарядов ядра. Таким образом, каждый химический элемент должен характеризоваться целым числом Z, названным атомным номером, который, как было замечено позже, оказался порядковым номером элемента в периодической системе.
Почти вся масса атома сосредоточена в ядре, составляющем центральную область системы радиусом 10-12-10-13 сантиметров. Электроны же являются очень легкими частицами, масса которых в 1836 раз меньше массы протона - ядра самого легкого атома - атома водорода (Z = 1). Заряд протона равен заряду электрона, но противоположен по знаку. За водородом в периодической системе следует гелий. Заряд ядра атома гелия в два раза больше заряда протона (Z = 2), а масса ядра в четыре раза больше массы протона. Заряд и масса ядра возрастают вместе с атомным номером химического элемента. Так, атомный номер урана 92. Ядро атома урана имеет электрический заряд, в 92 раза больший, чем^ заряд протона, а атомный вес его близок к 238.
Модель атома Резерфорда была принята в науке, так как имела несомненные преимущества перед моделью Томсона, которая не согласовывалась с достоверными данными, полученными в опытах Резерфорда, Марсдена, Гейгера и Чедвика по рассеянию альфа-частиц. Однако и в этой новой модели очень скоро обнаружились серьезные недостатки. Особенно это относилось к истолкованию явлений, происходящих в периферической области, т. е. там, где движутся электроны. Было еще очень много противоречий, объяснявшихся, как это обычно бывает, тем, что некоторые другие области физики еще не получили достаточного развития, чтобы привлечь их к объяснению явлений, понимание которых было связано с большими трудностями. Кроме того, не было еще необходимого количества опытного материала. Например, тогда еще нельзя было представить себе ядро как сложную динамическую систему, так как не был открыт нейтрон, входящий вместе с протоном в состав ядра. Резерфорд, развивая свою теорию рассеяния альфа-частиц, полагал, что между ними и ядрами действуют только кулоновские силы, тогда как на самом деле кроме кулоновских сил у поверхности ядра действуют особые ядерные силы, обнаруженные самим Резерфордом гораздо позже.
Но мы рассмотрим лишь главное противоречие в модели атома, которое отчетливо видел сам Резерфорд.
Согласно единственной известной в те годы классической электродинамике Максвелла, электрон не мог бесконечно обращаться вокруг ядра, так как вращаясь он должен был излучать энергию в виде периодически меняющегося электромагнитного поля и в конце концов упасть на ядро. Резерфорд не мог разрешить этого противоречия, что создавало трудное положение в дальнейшем развитии его идей и давало повод многим ученым, которые не могли внести конструктивных предложений, избавляющих от этой трудности оспаривать их правильность.
Но прежде чем рассказать о том, как противоречия, встретившиеся в объяснении движения электронов, были разрешены Нильсом Бором, необходимо напомнить, что с созданием планетарной модели атома открылась возможность разделять физические и химические свойства вещества. Было установлено, что большей частью первые определяются ядром атома, а вторые зависят от распределения электронов, связанных с ядром, но расположенных на очень больших расстояниях от него по сравнению с размером самого ядра.
Нильс Бор приехал к Резерфорду в Манчестер осенью 1911 г., чтобы получить у него разрешение присоединиться к группе его сотрудников весной 1912 г. после окончания занятий в Кембридже, где Бор проходил практику у Томсона после окончания Копенгагенского университета.
Бор отмечает, что незадолго до его приезда Резерфорд уже успел побывать в Брюсселе на открытии Сольвеев-ского конгресса, где впервые встретился с Планком и Эйнштейном.
Сольвеевский конгресс был международным совещанием ученых, организованным на личные средства Эрнеста Сольве (1838-1922), известного бельгийского инженера, изобретателя аммиачного способа промышленного производства соды. На этом конгрессе рассматривались наиболее важные проблемы науки. Первое совещание происходило в зале брюссельского отеля "Метрополь" под председательством прибывшего из Голландии Лоренца. В нем приняли участие многие выдающиеся ученые из разных стран: Макс Планк, Альберт Эйнштейн, Мари Кюри, Жан Перрен, Луи де Бройль, Вальтер Нернст, Джине, Каммерлинг-Оннес, Пуанкаре, Зоммерфельд, Вин, Варбург, Гольдшмидт, Бриллюэн. Каждое из этих имен было широко известно мировой научной общественности. Резерфорд представлял на этом совещании новую созданную им науку - ядерную физику.
А. Ф. Иоффе, состоявший членом комитета Сольвеевских конгрессов, собиравшихся в дальнейшем регулярно один раз в три года, отмечал в своих воспоминаниях, что участвовавший на этих конгрессах Резерфорд "был больше наблюдателем, но по спорным вопросам к нему обращались как к высшему авторитету". В более поздние годы в Сольвеевских конгрессах постоянно принимали участие многие крупнейшие специалисты по ядерной физике, например Ферми, Ирен и Фредерик Жолио-Кюри, Лиза Мейтнер.
Резерфорд согласился принять Бора в свою лабораторию, и таким образом датский ученый присоединился к манчестерской группе, интересы которой в то время были сосредоточены на исследованиях многих проблем, возникших как следствие открытия Резерфордом атомного ядра.
Бор писал о первых своих впечатлениях о манчестерской лаборатории: "В это время вокруг Резерфорда группировалось большое число молодых физиков из разных стран мира, привлеченных его чрезвычайной одаренностью как физика и редкими способностями как организатора научного коллектива. Хотя Резерфорд был всегда поглощен ходом своих собственных работ, у него все же хватало терпения выслушивать каждого из этих молодых людей, если он ощущал у них наличие каких-то идей, какими бы скромными с его собственной точки зрения они ни. казались".
Бор, которого, как и Эйнштейна, называют величайшим физиком-теоретиком XX века, по совету Резерфорда начал с того, что прослушал в манчестерской лаборатории курс экспериментальных методов исследований радиоактивности под руководством Гейгера, Маковера и Марс-дена.
Знакомство с постоянно совершенствующимися средствами физического эксперимента, конечно, было полезно и для физика, намеревавшегося заняться даже чисто теоретическими исследованиями. Проникновение в атом было бы невозможно без остроумных приборов и методов, разрабатывающихся Резерфордом на протяжении всей его жизни и составляющих один из важнейших элементов его научных успехов.
Так на смену спинтарископу с люминесцирующим экраном, с помощью которого Резерфорд сделал важные открытия и, в частности, изучил вместе со своими сотрудниками рассеяния альфа-частиц, пришел ионизационный счетчик заряженных частиц, получивший известность как счетчик Гейгера, хотя идея его принадлежала Резерфорду. Резерфорд предложил ее Гейгеру сразу после своего приезда в Манчестер, а затем вместе с Гейгером участвовал в разработке конструкции этого совершенного прибора. Счетчики Гейгера и сейчас широко применяют в научных исследованиях и на практике, например в таких обыденных делах, как проверка на радиоактивность рыбы. Счетчики Гейгера широко используются во Г всех отраслях современной атомной науки, техники и энергетики. Действие счетчика основано на явлении ионизации газов, которое изучал Резерфорд совместно с Томсоном в конце прошлого века, еще до открытия радиоактивности.
В 1911 г. старый друг Резерфорда профессор Кембриджского университета Чарлз Вильсон создал еще более удивительный прибор, с помощью которого можно было видеть следы отдельных альфа-частиц, названных физиками треками.
Резерфорд очень высоко оценил возможности нового прибора, названного камерой Вильсона. Во время ежегодного обеда, устраиваемого по традиции в Кавендишской лаборатории, Резерфорд, приехавший из Манчестера, произнес небольшую речь, которая, по словам присутствовавшего на обеде Нильса Бора, была проникнута почти детской радостью от того, что можно было буквально видеть (в камере Вильсона) рассеяние альфа-частиц на большие углы.
В камере Вильсона содержится воздух, насыщенный водяным паром. Движением поршня производят мгновенное расширение воздуха; воздух охлаждается и пар становится пересыщенным. Стремясь сконденсироваться, пар еще некоторое время способен сохранить состояние пересыщения. Пролетающая сейчас через камеру альфа-частица на своем пути отрывает от атомов, входящих в молекулы воздуха, электроны. Образующиеся ионы становятся центрами конденсации: пересыщенный водяной пар собирается на них в виде маленьких капель. Так, вдоль всего пути альфа-частицы возникает тонкий след из капелек воды, дающий исследователю четкое изображение траектории движения частицы - трека.
Наибольшее восхищение у Резерфорда (он сказал об этом в своей речи) вызывала настойчивость, с которой Вильсон продолжал исследования по образованию тумана со все более и более совершенными приборами.
Оценка, данная Резерфордом камере Вильсона, которую однажды он назвал даже "самым оригинальным и удивительным инструментом в истории науки", стала глубоко понятна лишь сейчас, когда развитие идеи Вильсона (т. е. использование частиц-ионов в качестве центров конденсации) привело к созданию гораздо более совершенных приборов. Этому развитию, как часто бывает, способствовало стремление исследователей устранить существенный недостаток первоначальной камеры Вильсона, а именно малый период действия. Он объяснялся тем, что пересыщение можно было создать на короткий промежуток времени. Затем требовалось подготовить камеру для дальнейшей работы, на что затрачивалось от 15 до 30 минут.
Необходимо было усовершенствовать камеру Вильсона, чтобы она могла действовать непрерывно. Новая камера получила название диффузионной. Верхняя крышка диффузионной камеры нагревается, а нижняя охлаждается, и таким образом поддерживается разность температур крышек (торцовых стенок). Газ, переходящий от теплой крышки к холодной, становится пересыщенным, и область пересыщения существует постоянно. Непрерывность действия диффузионной камеры позволяет регистрировать в ней треки частиц, образующиеся при редких ядерных столкновениях. Такие редкие события в мире ядер и элементарных частиц, конечно, нельзя было бы наблюдать в камере Вильсона, работающей с большими паузами. Но принципы действия той и другой одинаковы. Толщина пересыщенного слоя (зоны) диффузионной камеры невелика, но, увеличив площадь крышек, можно тем самым увеличить объем камеры. Уже построены диффузионные камеры с площадью крышек в несколько квадратных метров.
Еще более совершенной является пузырьковая камера, изобретенная Глезером в 1952 г., т. е. более чем через 40 лет после того, как камера Вильсона стала незаменимым орудием исследований Резерфорда. Принцип действия этой камеры тоже сходен с принципом, предложенным Вильсоном. Жидкость, наполняющая рабочий объем камеры, перегрета и способна к вскипанию при возникновении трека частицы с сильной ионизацией. Пузырьковую камеру физики шутливо называют "антикамерой Вильсона", имея в виду, что процессы, происходящие в них (кипение и конденсация), противоположны. Однако в обоих случаях наблюдатели видят треки частиц, обозначенные на ионном следе.
Пузырьковые камеры наполняют различными жидкостями, например метиловым спиртом, бензолом, бутаном, фреоном. Особенно хорошие результаты достигнуты в камере с жидким водородом. Этот наполнитель позволяет непосредственно регистрировать ядерные процессы между частицей, попадающей в камеру, и протонами (ядрами наполнителя). Большими преимуществами пузырьковой камеры является большая плотность регистрирующей среды, простота наблюдений (трек представляет собой последовательность пузырьков), быстрота подготовки к новой серии исследований: всего несколько секунд. Пузырьковые камеры сейчас применяются во всех лабораториях, где изучают частицы высоких энергий. Они часто изготовляются очень больших размеров. Например, в Физическом институте Академии наук СССР имеется пузырьковая камера объемом в 570 литров. При помощи таких камер уже сделаны многие важные открытия в физике элементарных частиц. Так, в 1962 г. в Дубне в лаборатории академика В. И. Векслера в водородной пузырьковой камере удалось зарегистрировать рождение античастицы - антиксигиперона.
Таков путь развития камеры Вильсона за несколько десятилетий. Восхищаясь первой конструкцией камеры, созданной его другом, Резерфорд, как гениальный экспериментатор, несомненно, чувствовал не только настоящее, но и будущее этого прибора.
Точно такой же была судьба широко применявшегося Резерфордом для исследования альфа-частиц метода сцинтилляций. Этот метод позволил Резерфорду открыть ядерную структуру атомов. Он основан на способности некоторых веществ - сцинтилляторов давать световую вспышку при ударе о них частиц. В настоящее время этот метод значительно усовершенствован. Современные сцинтилляционные счетчики, так же как и ионизационные ка-; меры, широко используются в экспериментальной ядерной физике. Кроме заряженных частиц они способны регистрировать также нейтроны и гамма-кванты. Сцинтилляционные счетчики состоят из двух основных частей: сцинтиллятора, т. е. вещества, испускающего кванты света при прохождении частиц, и прибора, фиксирующего их,- фотоумножителя (Резерфорд фиксировал вспышки визуально - глазом). Эффективность регистрации частиц сильно растет при увеличении объема сцинтиллятора. Поэтому сейчас уже построены счетчики с объемом сцинтиллятора до нескольких кубических метров. Для просмотра такой большой площади регистрирующего вещества применяются по несколько десятков фотоумножителей.
Таким образом, метод сцинтилляционной регистрации частиц, широко использованный Резерфордом, не только привел его к крупным открытиям, но и сейчас служит средством тончайших и сложнейших физических исследований.
Более полувека назад, когда камера Вильсона появлялась в физических лабораториях как новинка экспериментальной техники, она, естественно, вызывала восхищение ученых. Резерфорд же первый понял, что этот прибор сыграет большую роль в изучении атомов и ядер. Многих физиков интересовал вопрос о том, как Вильсона осенила идея использовать туман, чтобы увидеть пути частиц.
Чарлз Вильсон рассказывал Бору, что интерес к исследованию явления образования тумана впервые пробудился в нем, когда еще юношей он наблюдал появление и исчезновение туманов по мере того, как потоки воздуха поднимались на гребни Шотландских гор и затем вновь опускались в долины.
Вильсон первый получил фотоснимки треков альфа-частиц, представляющих прямые линии. Эти классические снимки и сейчас еще часто воспроизводятся в учебниках физики.
В камере Вильсона также наблюдали, что большинство альфа-частиц движется прямолинейно и только в некоторых местах их пути появляются острые изломы. Было ясно, что здесь частица встретилась с каким-то препятствием и поэтому ее путь резко искривился: возник излом следа. Произошло то же, что отметил Марсден, наблюдая рассеяние альфа-частиц в спинтарископе, а именно, что некоторые альфа-частицы не проходили через металлическую пластинку, поставленную на их пути, а отскакивали от нее.
Познакомившись с новыми методами исследования атома и атомного ядра, а также с результатами экспериментальных исследований, полученными Резерфордом и его сотрудниками, Нильс Бор занялся теоретическими исследованиями. Он уже имел некоторый опыт, полученный в Кембридже, где он был сильно увлечен оригинальными идеями Томсона, касающимися электронного строения атомов.
С самого начала работы в Манчестере Бору было ясно, что если принять модель атома Резерфорда, то никакими способами нельзя будет согласовать устойчивость системы ядро-электроны с классическими принципами механики и электродинамики. "Действительно,- писал Бор,- согласно механике Ньютона, никакая статическая система точечных зарядов не может находиться в устойчивом равновесии, а любое движение электронов вокруг ядра, согласно электродинамике Максвелла, связано с диссипацией* энергии через излучение; диссипация энергии в свою очередь ведет к постоянному уменьшению размеров системы; в конце концов это приводит к тесному сближению ядра и электронов внутри области, размеры которой значительно меньше, чем размеры самого атома".
* (Диссипация - рассеяние.- Прим. авт.)
Ограниченность классических теорий была подмечена самим Планком еще в 1900 г., когда он столкнулся с характерной прерывистостью, свойственной многим природным явлениям. Планк смог обосновать открытый им закон излучения (он рассматривал черное тело, излучающее интенсивнее всех других тел), лишь сделав смелое допущение, что энергия колебания атомов принимает не непрерывные значения, как это должно было быть по классическим представлениям, а может иметь ряд вполне определенных значений.
Дальнейшие исследования показали, что прерывистость присуща также излучению, что свет состоит из отдельных квантов, хотя до этого его считали волновым процессом. Планк установил, что свет с частотой колебания v должен поглощаться и испускаться в квантах энергии, величина которых пропорциональна V, поэтому он их принял равными hv. Входящая сюда постоянная величина h называется планковским квантом действия, или постоянной Планка. Ко времени открытия структуры атома среди физиков независимо от экспериментальных данных относительно этой структуры уже существовало убеждение, что квантовые представления сыграют большую роль в решении всей проблемы атомного строения вещества. И действительно, к тому времени уже были попытки использовать идеи Планка для объяснения движения электронов в модели Томсона.
Бор применил идею о прерывности к модели атома Резерфорда, сделав допущение, что атом может пребывать сколь угодно долго в совершенно определенных состояниях, характеризующихся своими орбитами электронов. Этим орбитам отвечали энергетические уровни электронов (в стационарных состояниях атомы, не излучая, могут находиться длительное время). Таким образом, согласно теории Бора электроны в атоме (рассматривался атом водорода) могут находиться лишь на определенных "разрешенных" орбитах. При переходе электрона с одной орбиты на другую происходит излучение или поглощение светового кванта. Иначе говоря, атом может существовать лишь в некоторых квантовых энергетических состояниях Е1, Е2, Е3 ... и каждый переход из какого-либо данного состояния Еi в Ef с меньшей энергией сопровождается испусканием излучения, частота которого v определяется формулой
Ei - Ef = hν
где h - постоянная Планка.
Теория Бора объясняла стабильность атома Резерфорда с помощью рабочей гипотезы, однако она не могла рассматриваться как последовательная физическая теория. Понадобилось еще 10 лет, чтобы познать законы, согласно которым построена электронная оболочка атома.
Бор рассказывал, что, когда он сообщил Резерфорду о разработанном им в Копенгагене квантовом варианте планетарной модели атома, "Резерфорд не сказал, что это глупо, но он никак не мог понять, каким образом электрон, начиная прыжок с одной орбиты на другую, знает, какой квант нужно ему испускать. Я ему говорил, что это как "branching ratio"* при радиоактивном распаде, но это его не убедило".
* (Под "branching ratio" имеют в виду вероятность испускания альфа- и бета-частиц в конкурирующих альфа- и бета-распадах: в этом случае употребляют выражения: вероятность распада, коэффициент разветвления, относительная вероятность распада и т. д. )
Модель атома Резерфорда - Бора совершенствовалась и была преобразована после появления волновой, или квантовой, механики. Началом ее послужила идея Луи де Бройля, выдвинутая им в 1924 г. Дуализм, благодаря которому свет может рассматриваться в одно и то же время как поток материальных частиц и волновое распространение энергии электромагнитного поля, согласно де Бройлю свойство не только света, но и всякого движения, в том числе движения вещества.
Идеи де Бройля вдохновили молодых теоретиков Эр-вина Шредингера из Цюриха и Вернера Гейзенберга из Геттингена на разработку квантовой теории. Они завершили свою работу в 1926 г. А еще через два года Поль Дирак в Кембридже создал релятивистскую квантовую механику, согласующуюся с теорией относительности. Представление о собственном вращении электронов (спин) получило четкое математическое выражение. Кроме того, после открытия Андерсоном и Блеккетом позитрона, теоретически предсказанного дираковской квантовой механикой, в науке окончательно утвердился факт существования античастиц. Впоследствии экспериментальное открытие антипротона и антинейтрона позволило наглядно показать, что античастицы имеют массу, равную массе самой частицы, но противоположный электрический заряд и противоположную ориентацию магнитного момента относительно спиновой оси.
Подобные фундаментальные открытия в теории, способствовавшие удивительному прогрессу наших знаний об атомной структуре вещества, в конце концов, обязаны открытию ядра Резерфордом. На любой стадии исследований ядерной физики это замечательное открытие всегда властно звало ученых вперед.
После опубликования квантовой теории атома водорода Бором Альберт Эйнштейн сказал, что все это ему очень понятно и близко тому, что он сам мог бы сделать. Но если это правильно, то физика как наука кончилась. Что хотел сказать этим великий ученый, трудно объяснить сейчас; вероятно, Эйнштейн имел в виду старую, доквантовую физику.
Представления, при помощи которых Бору удалось впервые приближенно объяснить устойчивость системы ядро - электроны, еще долго подвергались сомнению. Поэтому, когда Джине в сентябре 1913 г. выступил на ежегодном собрании Британской Ассоциации содействия прогрессу с докладом о модели атома, основанной на квантовых законах, произошел "инцидент", позабавивший Резерфорда, Бора и других сторонников квантовой теории.
Во время прений Джозеф Лармор торжественно предложил председателю собрания лорду Релею высказаться по поводу новых квантовых идей, предложенных для объяснения модели атома Резерфорда. Релей ответил так: "Когда я был молод, я неукоснительно исповедовал некоторые принципы, согласно одному из которых человек, переваливший за шестьдесят, не должен высказываться по поводу новых идей. Хотя я должен признаться в том, что я теперь придерживаюсь его не столь строго, однако в достаточной степени для того, чтобы не принимать участия в этой дискуссии!".
Релей в самом деле не одобрял квантовой механики и не верил, что "природа ведет себя таким образом". Он публично, правда в дипломатической форме, заявил о квантовой теории: "У меня есть трудности в принятии этого, как картины, которая действительно имеет место".
Известный физик-теоретик Пауль Эренфест, учитель Энрико Ферми, работавший в Петербурге, а затем в Лейдене, в двадцатых годах еще убеждал некоторых ученых поверить в квантовую механику. По поводу его иронического отношения к противникам этого нового учения советский физик Я. И. Френкель писал из Геттингена в 1925 г.: "... в середине июня собирается приехать Эренфест со свитой своих сотрудников и в том числе с цейлонским попугаем, обученным им произносить следующую фразу: "Aber meine Herren, das ist keine Physik" ("Но, господа, это не физика"). Этого попугая Эренфест выдвигает в председатели на предстоящих дискуссиях о новой квантовой механике".
Теоретические представления квантовой механики оказались гораздо менее наглядными, чем законы прочно утвердившихся классической механике Ньютона и электродинамики Максвелла.
Но если вернуться к работам Бора по приложению квантовой теории к модели атома Резерфорда, то следует сказать, что на том же заседании Британской Ассоциации содействию прогресса в Бирмингеме, на котором лорд Релей не одобрил этой теории, присутствовали такие крупнейшие научные авторитеты, как Мари Кюри, Лоренц, Лармор. Они вместе с Джинсом поддерживали идеи Бора. С этих пор, собственно, началось быстрое развитие квантовой механики, которой заинтересовались некоторые теоретики в различных странах и, конечно, прежде всего работавшие с Резерфордом.
Летом 1913 г. Бор в Кавендишской лаборатории обсуждал с учениками Резерфорда Георгом Хевеши и Генри Мозли вопрос о том, что расположение элементов в периодической системе должно происходить по мере увеличения их атомного номера. Чтобы выяснить этот вопрос Мозли решил измерить высокочастотные спектры элементов методами Лауэ-Брегга.
В результате серии систематических измерений Мозли открыл простой, но очень важный закон, позволяющий однозначно приписать атомный номер элементу на основании его высокочастотного спектра.
Закон Мозли убедительно подтвердил правильность представления Резерфорда о планетарном строении атома и вместе с тем обнаружил, по словам Бора, потрясающую интуицию Менделеева, который в определенных местах своей таблицы отошел от правильной последовательности возрастания атомных весов, т. е. от основного принципа построения периодической системы элементов. Закон Мозли оказался, в частности, безошибочным ориентиром при поисках еще не открытых элементов, соответствующих вакантным местам в последовательности атомных номеров. Работа Мозли послужила также началом существенного прогресса в изучении электронных оболочек атомов и их взаимодействий с ядрами.
В начале первой мировой войны 1914 г. манчестерская группа Резерфорда почти полностью распалась. Сотрудники лаборатории были мобилизованы в армию и отправлены в Европу и в другие районы для участия в боевых действиях.
Резерфорд и его жена в это время находились в Америке, где они остановились на пути из Новой Зеландии в Англию.
После возвращения в Манчестер, Резерфорд, как и многие другие английские ученые и специалисты, должен был включиться в работу по военным проблемам. По заданию военного ведомства он приступил к разработке акустических приборов для обнаружения подводных лодок. Этим приборам придавалось большое значение в связи с необходимостью усилить борьбу с немецкими подводными лодками, наносившими большой ущерб военным и торговым кораблям английского флота. (Любопытно, что в годы второй мировой войны эта проблема нисколько не утратила своей остроты и ученик Резерфорда - Чедвик - был привлечен английским правительством к разработке приборов для обнаружения подводных лодок; правда, это были уже не акустические, а радиоэлектронные приборы, получившие название радаров.)
В мае 1917 г. Резерфорд был командирован в Париж для участия в совещании во Французском адмиралтействе, на котором обсуждались новые методы акустического обнаружения подводных лодок, разрабатывавшиеся его другом Ланжевеном. Резерфорд присутствовал в лаборатории Ланжевена в Коллеж де Франс при проведении некоторых экспериментов по возбуждению ультразвуковых волн с помощью пьезокварцевых излучателей, созданных Ланжевеном.
Работа по заданию военного ведомства отнимала у Резерфорда много времени и заставила его поэтому передать чтение лекций студентам своим близким сотрудникам Бору, Эвансу и Маковеру. Только очень малую часть времени Резерфорд мог использовать для продолжения собственных исследований, среди которых больше всего его занимала возможность произвести с помощью альфа-частиц разрушение ядра. Подобный процесс тогда мог казаться почти невероятным, но Резерфорд пришел к выводу, что попытка вызвать его не безнадежна.
Чрезмерная занятость в военные годы тем не менее не могла заставить Резерфорда отказаться от установившейся еще до войны традиции регулярно раз в месяц собираться с близкими друзьями для обсуждения различных проблем науки, политики, общественной жизни. Бор, участвовавший в этих интересных беседах, писал, что в них неизменно принимали участие философ Александер, историк Тоут, антрополог Элиот Смит и химик X. Вейцман. Весной 1916 г. Нильс Бор уехал в Копенгаген и оттуда поддерживал связь с Резерфордом.
Бурно протекавшие военные события определяли судьбу многих учеников и сотрудников Резерфорда, мобилизованных в действующую армию; в лучшем случае они были полностью устранены из сфер науки, став на многие годы обезличенными солдатами и офицерами на полях сражений.
Марсден сражался на передовой линии фронта во Франции. Чедвик к концу войны был захвачен немцами и заключен в концлагерь для военнопленных. Особенно трагична была судьба талантливого Генри Мозли, который погиб в 1917 г. в возрасте 28 лет. Резерфорд был потрясен гибелью своего любимого ученика, которого он до этого безуспешно пытался перевести с фронта на работу в военную промышленность.
О своих исследованиях, которые ему приходилось проводить теперь без сотрудников, Резерфорд писал Бору в Копенгаген (9 декабря 1916 г.): "Время от времени мне удается урвать свободные полдня, чтобы провести некоторые из моих собственных экспериментов, и я думаю, что получил результаты, которые в конце концов окажутся чрезвычайно важными. Мне очень хотелось бы обсудить все эти вещи вместе с вами здесь. Я обнаруживаю и подсчитываю легкие атомы, приводимые в движение альфа-частицами, и эти результаты, как мне кажется, проливают яркий свет на характер и распределение сил вблизи ядра. Я также пытаюсь этим же методом взломать атом. В одном из опытов результаты представляются обнадеживающими, но потребуется уйма работы, чтобы их подтвердить. Кей помогает мне и в настоящее время является специалистом по подсчетам".
В июле 1919 г. Бор приехал из Копенгагена в Манчестер. Резерфорд рассказал ему, что он должен принять важное решение в связи с предложением занять должность профессора Кавендишской лаборатории Кембриджского университета. Резерфорду было трудно решиться расстаться с манчестерской лабораторией, где ученый долго и плодотворно работал, но он, конечно, не мог отказаться от приглашения стать руководителем Кавендишской лаборатории, заняв место, как говорил Бор, в непревзойденной плеяде кавендишских профессоров.
|
ПОИСК:
|